题目内容
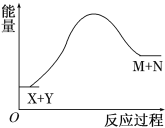
【题目】已知X+Y![]() M+N反应中的能量变化过程如图,则下列有关说法正确的是
M+N反应中的能量变化过程如图,则下列有关说法正确的是
A. X的能量一定低于M的能量,Y的能量一定低于N的能量
B. 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量
C. 因为该反应为吸热反应,故一定要加热反应才能进行
D. 加入催化剂,可减小M+N与X+Y间的能量差
【答案】B
【解析】
A.反应热取决于反应物与生成物的总能量,而不是某一种反应物或生成物的能量关系;
B.反应物的总能量低于生成物的总能量时反应是吸热反应;
C.吸热反应不一定在加热的条件下发生;
D.催化剂能降低反应的活化能,不改变反应热。
A.由图可知,反应物的总能量低于生成物的总能量,不能说明X的能量一定低于M的能量,Y的能量一定低于N的能量,选项A错误;
B、由图可知,反应物的总能量低于生成物的总能量,X+Y![]() M+N是一个吸热反应,则破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量,选项B正确;
M+N是一个吸热反应,则破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量,选项B正确;
C、吸热反应不一定在加热的条件下发生,比如氯化铵和Ba(OH)2·8H2O的反应是吸热反应,但常温下就能发生,选项C错误;
D、催化剂能降低反应的活化能,不改变反应热,加入催化剂,M+N与X+Y间的能量差不变,选项D错误;
答案选B。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案【题目】已知某化学反应的平衡常数表达式为![]() ,在不同的温度下该反应的平衡常数如下表:
,在不同的温度下该反应的平衡常数如下表:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述不正确的是( )
A. 若在1 L的密闭容器中通入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO2为0.4 mol时,该反应达到平衡状态
B. 上述反应的正反应是放热反应
C. 该反应的化学方程式是CO(g)+H2O(g) ![]() CO2(g)+H2 (g)
CO2(g)+H2 (g)
D. 若平衡浓度符合下列关系式:![]() ,则此时的温度为1000 ℃
,则此时的温度为1000 ℃