题目内容
7.现有100mL Na2CO3、Na2S04的混合溶液,分为两等份,一份加入足量的盐酸,产生的气体全部被澄清石灰水吸收,得到0.50g白色沉淀,另一份加入足量的盐酸酸化的BaCl2溶液,得到白色沉淀2.33g,试求:(1)原混合溶液中各物质的物质的量浓度;
(2)原混合溶液中Na+的物质的量浓度.
分析 (1)生成0.50g白色沉淀为碳酸钙,根据碳原子守恒计算出碳酸钠的物质的量;加入足量的盐酸酸化的BaCl2溶液后生成的2.33g沉淀为硫酸钡,根据硫原子守恒计算出硫酸钠的物质的量,每份溶液的体积为50mL,最后根据c=$\frac{n}{V}$计算出碳酸钠、硫酸钠的物质的量浓度;
(2)根据碳酸钠、硫酸钠的浓度及钠离子守恒计算出原混合液中钠离子的物质的量浓度.
涉及离子反应有Ba2++SO42-═BaSO4↓、Ba2++CO32-═BaCO3↓、BaCO3+2H+═Ba2++CO2↑+H2O.
解答 解:(1)一份加入足量的盐酸,产生的气体全部被澄清石灰水吸收得到0.50g白色沉淀为碳酸钙,碳酸钙的物质的量为:$\frac{0.50g}{100g/mol}$=0.005mol,根据碳原子守恒可知每份溶液中含有碳酸钠的物质的量为0.005mol,其浓度为:c(Na2CO3)=$\frac{0.005mol}{0.05L}$=0.1mol/L;
另一份加入足量的盐酸酸化的BaCl2溶液,得到白色沉淀2.33g为硫酸钡,生成的硫酸钡的物质的量为:$\frac{2.33g}{233g/mol}$=0.01mol,根据硫酸根离子守恒可知每份溶液中含有硫酸钠的物质的量为0.01mol,硫酸钠的浓度为:c(Na2S04)=$\frac{0.01mol}{0.05L}$0.2mol/L,
答:原混合溶液中碳酸钠的浓度为0.1mol/L,硫酸钠的浓度为0.2mol/L;
(2)溶液具有均一性,根据钠离子守恒可知原混合液中钠离子浓度为:c(Na+)=2c(Na2CO3)+2c(Na2S04)=0.1mol/L×2+0.2mol/L×2=0.6mol/L,
答:原混合液中钠离子的物质的量浓度为0.6mol/L.
点评 本题考查混合物的有关计算,题目难度中等,明确发生的反应实质为解答关键,注意根据守恒思想在化学计算中应用方法,试题培养了学生的化学计算能力.

①加入稀硫酸有气泡产生 ②加入稀硫酸后,没有气泡生成 ③加入稀硫酸后,溶液中有红色不溶物出现 ④插入溶液中铁片表面有红色物质析出.
| A. | 只有②③ | B. | 只有③④ | C. | 只有④ | D. | ①②③④ |
| A. | Na+、Mg2+、Al3+、Cl- | B. | Na+、K+、Cl-、SO42- | ||
| C. | HCO3-、Na+、Cl-、K+ | D. | I-、Fe2+、Na+、NO3- |
 某温度时,在2L密闭容器中有X、Y、Z三种气态物质,实验测得不同时刻各物质的量如下表所示,同时测得至3min时吸收热量75kJ.
某温度时,在2L密闭容器中有X、Y、Z三种气态物质,实验测得不同时刻各物质的量如下表所示,同时测得至3min时吸收热量75kJ. | t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.60 | 0.20 | 0.80 |
| 14 | 0.60 | 0.20 | 0.80 |
(2)该温度下反应的平衡常数K=$\frac{1600}{9}$.
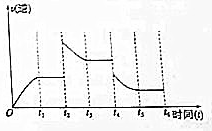
(3)若该反应的逆反应速率与时间的关系如图所示.则:
①t2~t3时平衡向逆(填“正”或“逆”)反应方向移动.
②t4时被改变的外界条件是B(选择一个正确选项)
A升温 B降温 C.降压 D.移去部分反应物 E加入负催化剂.
| A. | M+ | B. | HA- | C. | A2- | D. | M+和HA- |
| A. | PH=7,溶液一定显中性 | |
| B. | 当溶液c(H+)=c(OH-)时,溶液显中性 | |
| C. | 正盐溶液一定显中性,酸性盐溶液可能显酸性或碱性 | |
| D. | 当溶液显酸性时,水电离的c(H+)>c(OH-) |
 氮及其化合物在生产、生活中有极其重要的作用.
氮及其化合物在生产、生活中有极其重要的作用.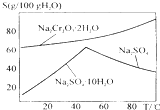 工业上以铬铁矿(主要成分FeO•Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7•2H2O)的主要反应如下:
工业上以铬铁矿(主要成分FeO•Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7•2H2O)的主要反应如下: