题目内容
【题目】图中,固体A是铁锈的主要成分. ![]()
请回答:
(1)固体A的化学式 .
(2)写出B﹣C的化学方程式
(3)写出D﹣E在溶液中发生离子方程式 .
【答案】
(1)Fe2O3
(2)2Fe+3Cl2 ![]() 2FeCl3
2FeCl3
(3)Ba2++SO42﹣=BaSO4↓
【解析】解:A是铁锈的主要成分是氧化铁,与一氧化碳反应生成单质铁和二氧化碳,铁与氯气反应生成氯化铁,所以固体C为氯化铁,氯化铁与二氧化硫与水反应生成硫酸亚铁,硫酸亚铁溶液中加入氯化钡生成白色沉淀硫酸钡,则E是硫酸钡.
(1.)固体A是铁锈的主要成分,化学式Fe2O3 , 所以答案是:Fe2O3;
(2.)一氧化碳还原氧化铁的化学方程式为:Fe2O3+3CO ![]() 2Fe+3CO2 , 单质B为Fe,铁和氯气发生反应生成固体C为氯化铁,反应的化学方程式为:2Fe+3Cl2
2Fe+3CO2 , 单质B为Fe,铁和氯气发生反应生成固体C为氯化铁,反应的化学方程式为:2Fe+3Cl2 ![]() 2FeCl3 ,
2FeCl3 ,
所以答案是:2Fe+3Cl2 ![]() 2FeCl3;
2FeCl3;
(3.)固体C和二氧化硫水溶液反应生成氯化亚铁、硫酸和盐酸,氯化铁与二氧化硫与水反应生成硫酸亚铁,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42﹣+4H+ , 溶液D和氯化钡溶液反应生成白色沉淀硫酸钡,Ba2++SO42﹣=BaSO4↓,所以答案是:Ba2++SO42﹣=BaSO4↓.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】Ι.用50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液中和反应过程中所放出的热量计算中和热 。
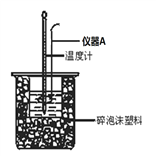
(1)烧杯间填满泡沫塑料的作用是___________________________________;
(2)大烧杯上若不盖硬纸板,求得的中和热数值______(填“偏大”、“偏小”、“无影响”)
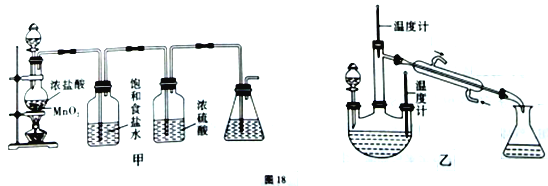
(3)如图所示,仪器A的名称是____________________;
(4)重复三次实验,记录的实验数据如下:
实验用品 | 溶液温度 | |||
t1 | t2 | |||
① | 50 mL 0.55 mol·L-1 NaOH溶液 | 50 mL 0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.3 ℃ |
② | 50 mL 0.55 mol·L-1 NaOH溶液 | 50 mL 0.5 mol·L-1 HCl溶液 | 20 ℃ | 25.5 ℃ |
③ | 50 mL 0.55 mol·L-1 NaOH溶液 | 50 mL 0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.5 ℃ |
已知:Q=cmΔt,反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。计算ΔH=___________kJ/mol
(5)实验中改用80mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等、“不相等”),所求中和热______(填“相等、“不相等”).
Ⅱ.某研究性学习小组设计了一组实验来探究元素周期律。甲同学一次性完成N、C、Si的非金属性强弱的比较;乙同学完成了氧元素的非金属性比硫强的实验。
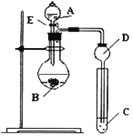
(1)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液②稀盐酸③碳酸钙④Na2SiO3 溶液⑤SiO2
试剂A为_________;试剂C为_________(填序号)
(2)乙同学设计的实验所用到试剂A为________;装置C中反应的化学方程式为___________________________。