题目内容
【题目】用6 g CaCO3与100 mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如右图所示。下列说法正确的是
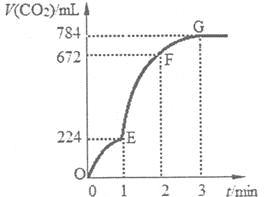
A. OE段表示的平均反应速率最快,可能的原因是该反应是放热反应
B. EF段用HC1浓度的减小表示的该反应的平均反应速率为0.2 mol/(L·min)
C. 在F点收集到的CO2的体积最大
D. 在G点以后收集的CO2的量不再增多,原因是稀盐酸已反应完全
【答案】D
【解析】试题分析:A、由图可知,1min时间内,EF段生成的二氧化碳的体积最多,故EF段反应速率最快,故A错误;B、由图可知EF段生成的二氧化碳体积为672mL-224mL=448mL,二氧化碳的物质的量为![]() =0.02mol,根据方程式CaCO3+2HCl=CaCl2+CO2↑+H2O可知,△n(HCl)=2n(CO2)=2×0.02mol=0.04mol,故用盐酸表示该反应的平均反应速率为
=0.02mol,根据方程式CaCO3+2HCl=CaCl2+CO2↑+H2O可知,△n(HCl)=2n(CO2)=2×0.02mol=0.04mol,故用盐酸表示该反应的平均反应速率为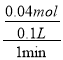 =0.4mol/(Lmin),故B错误;C、曲线上点的纵坐标的值即为该点收集的二氧化碳的体积,由图可知G点收集的二氧化碳最多,故C错误;D、根据反应CaCO3+2HCl=CaCl2+CO2↑+H2O,6 g CaCO3完全反应生成二氧化碳应该是1.344L,而G点是784ml,说明CaCO3未反应完,则盐酸完全反应,故D正确。故选D。
=0.4mol/(Lmin),故B错误;C、曲线上点的纵坐标的值即为该点收集的二氧化碳的体积,由图可知G点收集的二氧化碳最多,故C错误;D、根据反应CaCO3+2HCl=CaCl2+CO2↑+H2O,6 g CaCO3完全反应生成二氧化碳应该是1.344L,而G点是784ml,说明CaCO3未反应完,则盐酸完全反应,故D正确。故选D。

练习册系列答案
相关题目