题目内容
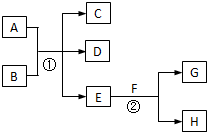 在如图各变化中,E为无色无味的液体(常温下),F为银白色金属,在空气中燃烧生成淡黄色固体,G为常见的无色气体(反应条件均已省略).回答下列问题:
在如图各变化中,E为无色无味的液体(常温下),F为银白色金属,在空气中燃烧生成淡黄色固体,G为常见的无色气体(反应条件均已省略).回答下列问题:(1)在实验室中,少量F保存在
(2)若A是一种强碱,D是一种无色气体,遇HCl气体能产生白烟,反应①在溶液中加热进行,则反应①中产生气体D的离子方程式是
(3)若反应①在加热条件下进行,单质A和化合物B按物质的量之比为1:2发生反应,且C、D是两种均能使澄清的石灰水变浑浊的无色气体,则反应①的化学方程式是
考点:无机物的推断
专题:推断题
分析:(1)F为银白色金属,在空气中燃烧生成淡黄色固体,则F为Na,E为无色无味的液体(常温下),与Na反应生成G与H,且G为常见的无色气体,则E为H2O,G为H2,H为NaOH;
(2)若A是一种强碱,D是一种无色气体,遇HCl气体能产生白烟,可推知D为氨气,反应①是铵盐与强碱反应;
(3)若反应①在加热条件下进行,单质A和化合物B按物质的量之比为1:2发生反应,且C、D是两种均能使澄清的石灰水变浑浊的无色气体,应碳与浓硫酸反应,可推知A为碳,B为硫酸,C为二氧化碳,D为二氧化硫,据此解答.
(2)若A是一种强碱,D是一种无色气体,遇HCl气体能产生白烟,可推知D为氨气,反应①是铵盐与强碱反应;
(3)若反应①在加热条件下进行,单质A和化合物B按物质的量之比为1:2发生反应,且C、D是两种均能使澄清的石灰水变浑浊的无色气体,应碳与浓硫酸反应,可推知A为碳,B为硫酸,C为二氧化碳,D为二氧化硫,据此解答.
解答:
解:(1)F为银白色金属,在空气中燃烧生成淡黄色固体,则F为Na,E为无色无味的液体(常温下),与Na反应生成G与H,且G为常见的无色气体,则E为H2O,G为H2,H为NaOH,则:
在实验室中,少量Na保存在煤油中,反应②的化学方程式为:2Na+2H2O═2NaOH+H2↑,
故答案为:煤油;2Na+2H2O═2NaOH+H2↑;
(2)若A是一种强碱,D是一种无色气体,遇HCl气体能产生白烟,可推知D为氨气,反应①是铵盐与强碱反应,反应①中产生氨气的离子方程式是:NH4++OH-
NH3+H2O,
故答案为:NH4++OH-
NH3+H2O;
(3)若反应①在加热条件下进行,单质A和化合物B按物质的量之比为1:2发生反应,且C、D是两种均能使澄清的石灰水变浑浊的无色气体,应碳与浓硫酸反应,可推知A为碳,B为硫酸,C为二氧化碳,D为二氧化硫,反应①的化学方程式是:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O.
在实验室中,少量Na保存在煤油中,反应②的化学方程式为:2Na+2H2O═2NaOH+H2↑,
故答案为:煤油;2Na+2H2O═2NaOH+H2↑;
(2)若A是一种强碱,D是一种无色气体,遇HCl气体能产生白烟,可推知D为氨气,反应①是铵盐与强碱反应,反应①中产生氨气的离子方程式是:NH4++OH-
| ||
故答案为:NH4++OH-
| ||
(3)若反应①在加热条件下进行,单质A和化合物B按物质的量之比为1:2发生反应,且C、D是两种均能使澄清的石灰水变浑浊的无色气体,应碳与浓硫酸反应,可推知A为碳,B为硫酸,C为二氧化碳,D为二氧化硫,反应①的化学方程式是:C+2H2SO4(浓)
| ||
故答案为:C+2H2SO4(浓)
| ||
点评:本题考查无机物推断,物质的颜色、状态及反应现象等是推断突破口,需要学生熟练掌握元素化合物性质,难度中等.

练习册系列答案
相关题目
苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )
①苯不能使溴水反应褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤苯是正六边形.
①苯不能使溴水反应褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤苯是正六边形.
| A、①②④⑤ | B、①③④⑤ |
| C、①②③④ | D、②③④⑤ |
下列叙述正确的是( )
| A、铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
| B、向FeBr2溶液中滴加少量氯水,溶液变浅黄色是因为生成了Br2 |
| C、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液,溶液褪色,说明BaCl2溶液有酸性 |
下列有关试验的做法不正确的是( )
| A、分液时,分液漏斗的上层液体应由上口倒出 |
| B、检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 |
| C、配置0.1000mol?L-1氢氧化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 |
| D、用加热分解的方法区分碳酸钠和碳酸氢钠两种固体 |