题目内容
10.(1)0.5mol NH3的质量是8.5g,在标准状况下的体积为11.2L;含9.03×1023个氢原子.(2)将标准状况下22.4L的HCl溶于水配成200mL的溶液,所得溶液的物质的量浓度为5mol/L;配制250mL 0.5mol•L-1氯化钠溶液,需要2mol•L-1的氯化钠溶液的体积是62.5mL.
分析 (1)根据m=nM计算氨气的质量,根据V=nVm计算氨气体积,氢原子物质的量为氨气的3倍,根据N=nNA计算氢原子数目;
(2)根据n=$\frac{V}{{V}_{m}}$计算HCl物质的量,再根据c=$\frac{n}{V}$计算HCl的物质的量浓度;根据稀释定律计算需要需要2mol•L-1的氯化钠溶液.
解答 解:(1)0.5mol NH3的质量是0.5mol×17g/mol=8.5g,在标准状况下的体积为0.5mol×22.4L/mol=11.2LL;含氢原子数目为0.5mol×3×6.02×1023mol-1=9.03×1023,
故答案为:8.5;11.2;9.03×1023;
(2)标准状况下22.4L HCl的物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,溶于水配成200mL的溶液,所得溶液的物质的量浓度为$\frac{1mol}{0.2L}$=5mol/L;
根据稀释定律,稀释前后溶质NaCl的物质的量不变,则配制250mL 0.5mol•L-1氯化钠溶液,需要2mol•L-1的氯化钠溶液的体积是$\frac{250mL×0.5mol/L}{2mol/L}$=62.5mL,
故答案为:5mol/L;62.5.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | NaHSO4在熔融状态下的电离方程式为NaHSO4═Na++H++SO42- | |
| B. | H2CO3是弱酸,故Na2CO3是弱电解质 | |
| C. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| D. | NaHCO3在水溶液中的电离:NaHCO3═Na++HCO3-、HCO3-?H++CO32- |
18.下列物质有两种或两种以上的同分异构体,其同分异构体中的某一种烃的一氯取代物只有一种,则这种烃可能是( )
| A. | 分子中具有7个碳原子的芳香烃 | B. | 分子中具有4个碳原子的烷烃 | ||
| C. | 分子中具有5个碳原子的烷烃 | D. | 相对分子质量为86的烷烃 |
5.下列说法正确的是( )
| A. | 淀粉、纤维素都属于纯净物 | B. | 金属氧化物都是碱性氧化物 | ||
| C. | 食醋、纯碱、食盐分别属于酸、碱、盐 | D. | 酸性氧化物不一定与水反应生成酸 |
15.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的是( )
| A. | 油脂都是高级饱和脂肪酸甘油酯,不能使溴的四氯化碳溶液褪色 | |
| B. | 糖类、脂肪和蛋白质都能发生水解反应 | |
| C. | 蔗糖和麦芽糖互为同分异构体,可以利用银氨溶液区别二者 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
2.有机物X是一种药物,结构简式如下.下列叙述不正确的是( )


| A. | X的分子式为C18H20O2 | |
| B. | 1molX最多能与7molH2发生加成反应 | |
| C. | X与NaOH溶液或NaHCO3溶液均能反应 | |
| D. | 1molX与饱和溴水混合,最多消耗5molBr2 |
19.下列物质的溶液在空气中放置一段时间,溶液的pH值会有下降现象的是(不考虑溶质挥发)( )
①H2S;②H2SO3;③浓H2SO4;④Na2CO3;⑤氯水;⑥Ca(OH)2;⑦Na2SO3.
①H2S;②H2SO3;③浓H2SO4;④Na2CO3;⑤氯水;⑥Ca(OH)2;⑦Na2SO3.
| A. | ②③⑤⑥⑦ | B. | ①②④⑤⑥ | C. | ②⑥⑦ | D. | ③④⑤⑦ |
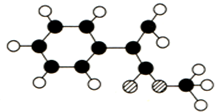 (图中球与球之间连线代表化学键单键或双键).
(图中球与球之间连线代表化学键单键或双键).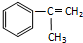 出发来合成M,路线如下:
出发来合成M,路线如下: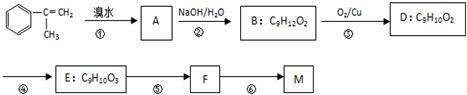
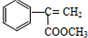 .
. .
. (注明反应条件).
(注明反应条件).