题目内容
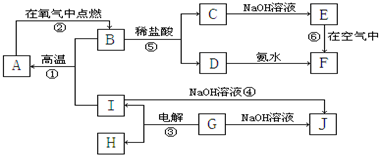
(2011?江西一模)A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素.
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第
(2)写出反应①的化学方程式
(3)写出D和J的水溶液反应的离子方程式
(4)写出反应③的电极方程式:阳极:
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是
(6)反应④中的氧化剂是
(7)B的化学式:

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第
四
四
周期、第Ⅷ
Ⅷ
族;(2)写出反应①的化学方程式
8Al+3Fe3O4
4Al2O3+9Fe
| ||
8Al+3Fe3O4
4Al2O3+9Fe
;
| ||
(3)写出D和J的水溶液反应的离子方程式
Fe3++3AlO2-+6H2O=Fe(OH)3+3Al(OH)3
Fe3++3AlO2-+6H2O=Fe(OH)3+3Al(OH)3
;(4)写出反应③的电极方程式:阳极:
6O2--12e-=3O2↑
6O2--12e-=3O2↑
;阴极:4Al3++12e-=4Al
4Al3++12e-=4Al
.(5)从能量变化的角度看,①②③反应中属于△H<0的反应是
①②
①②
.(填序号)(6)反应④中的氧化剂是
水
水
.(7)B的化学式:
Fe3O4
Fe3O4
,H的结构式:O=O
O=O
.分析:本题的突破口为E,E为C和NaOH的反应产物,则E为氢氧化物,且E能与空气反应生成另一种氢氧化物F,说明E为
Fe(OH)2,F为Fe(OH)3,则B为Fe3O4,A为Fe,C为FeCl2,D为FeCl3,Fe由I和Fe3O4在高温下反应生成,则应为铝热反应,所以I为Al,则G应为Al2O3,J为NaAlO2,H为O2,结合对应物质的性质解答该题.
Fe(OH)2,F为Fe(OH)3,则B为Fe3O4,A为Fe,C为FeCl2,D为FeCl3,Fe由I和Fe3O4在高温下反应生成,则应为铝热反应,所以I为Al,则G应为Al2O3,J为NaAlO2,H为O2,结合对应物质的性质解答该题.
解答:解:E为C和NaOH的反应产物,则E为氢氧化物,且E能与空气反应生成另一种氢氧化物F,说明E为Fe(OH)2,F为
Fe(OH)3,则B为Fe3O4,A为Fe,Fe由I和Fe3O4在高温下反应生成,则应为铝热反应,所以I为Al,则G应为Al2O3,J为
NaAlO2,H为O2,则
(1)A、B、C、D、E、F六种物质中所含同一种元素为Fe,原子序数为26,位于周期表第四周期第族Ⅷ,
故答案为:四;Ⅷ;
(2)反应①为铝热反应,由Al和Fe3O4在高温下反应,反应的化学方程式为8Al+3Fe3O4
4Al2O3+9Fe,
故答案为:8Al+3Fe3O4
4Al2O3+9Fe;
(3)FeCl3和NaAlO2的水溶液发生互促水解反应,反应的离子方程式为Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓,
故答案为:Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓;
(4)反应③为工业电解氧化铝制备铝的反应,阳极反应为6O2--12e-=3O2↑,阴极反应为4Al3++12e-=4Al,
故答案为:6O2--12e-=3O2↑;4Al3++12e-=4Al;
(5)①②③反应中,①为铝热反应,为放热反应,②为铁的燃烧,为放热反应,③为氧化铝的电解,为吸热反应,
故答案为:①②;
(6)反应④为铝和氢氧化钠溶液的反应,生成氢气,反应中水为氧化剂,
故答案为:水;
(7)B为Fe3O4,H为O2,结构式为O=O,
故答案为:Fe3O4; O=O.
Fe(OH)3,则B为Fe3O4,A为Fe,Fe由I和Fe3O4在高温下反应生成,则应为铝热反应,所以I为Al,则G应为Al2O3,J为
NaAlO2,H为O2,则
(1)A、B、C、D、E、F六种物质中所含同一种元素为Fe,原子序数为26,位于周期表第四周期第族Ⅷ,
故答案为:四;Ⅷ;
(2)反应①为铝热反应,由Al和Fe3O4在高温下反应,反应的化学方程式为8Al+3Fe3O4
| ||
故答案为:8Al+3Fe3O4
| ||
(3)FeCl3和NaAlO2的水溶液发生互促水解反应,反应的离子方程式为Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓,
故答案为:Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓;
(4)反应③为工业电解氧化铝制备铝的反应,阳极反应为6O2--12e-=3O2↑,阴极反应为4Al3++12e-=4Al,
故答案为:6O2--12e-=3O2↑;4Al3++12e-=4Al;
(5)①②③反应中,①为铝热反应,为放热反应,②为铁的燃烧,为放热反应,③为氧化铝的电解,为吸热反应,
故答案为:①②;
(6)反应④为铝和氢氧化钠溶液的反应,生成氢气,反应中水为氧化剂,
故答案为:水;
(7)B为Fe3O4,H为O2,结构式为O=O,
故答案为:Fe3O4; O=O.
点评:本题考查无机物的推断,题目难度较大,推断时,明确各物质的反应关系以及反应现象为解答该题的关键,答题时注意相关化学方程式的书写,为易错点.

练习册系列答案
相关题目