题目内容
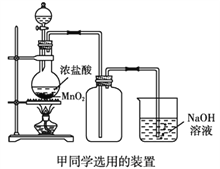
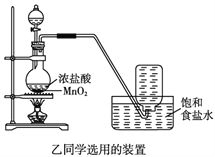
【题目】某同学欲在实验室中完成Fe与水蒸气反应的实验,实验装置如图甲、乙所示。
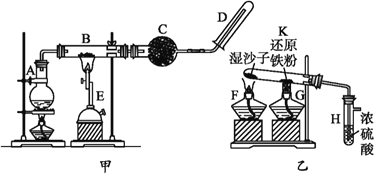
已知B中放入的是铁粉与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G 为带有铁丝网罩的酒精灯。对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?________________。
(2)乙装置中湿沙子的作用是________________。
(3)B处发生反应的化学方程式为_________________。
(4)该同学认为欲在乙装置的导管口处点燃反应产生的气体,装置H必不可少,H的作用是________________。
(5)对比甲、乙两装置的B和K,B的优点是____________。
【答案】 向H中加入水没过导管口,连接好装置,微热K,若H中导管口出现气泡,停止加热后导管中出现水柱,证明气密性良好(其他合理答案也可) 提供水蒸气 3Fe+4H2O(g)![]() Fe3O4+4H2 干燥氢气,降低H2中水蒸气的含量 使用石棉绒,增大水蒸气与铁粉的接触面积,使反应充分进行
Fe3O4+4H2 干燥氢气,降低H2中水蒸气的含量 使用石棉绒,增大水蒸气与铁粉的接触面积,使反应充分进行
【解析】考查实验方案设计与评价,(1)检查装置的气密性, 向H中加入水没过导管口,连接好装置,微热K,若H中导管口出现气泡,停止加热后导管中出现水柱,证明气密性良好;(2)此反应是铁与水蒸气的反应,湿沙子受热时,水蒸发产生水蒸气,即湿沙子的作用是提供水蒸气;(3)B处反应的是3Fe+4H2O(g)![]() Fe3O4+4H2;(4)潮湿的氢气很难燃烧,故H的作用是干燥氢气,降低H2中水蒸气的含量;(5)装置B中使用石棉绒可以增大水蒸气与铁粉的接触面积,使反应充分进行。
Fe3O4+4H2;(4)潮湿的氢气很难燃烧,故H的作用是干燥氢气,降低H2中水蒸气的含量;(5)装置B中使用石棉绒可以增大水蒸气与铁粉的接触面积,使反应充分进行。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。实验室用干燥而纯净的氯气和二氧化硫合成硫酰氯,装置如图所示(夹持仪器已省略)
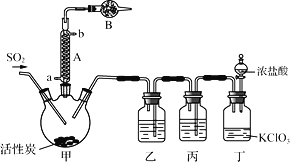
已知:①乙和丙装置作用为除去氯气中的杂质。
②氯气有毒,谨防泄漏,尾气需处理,不能随意排放。
③丁是制备氯气的装置。
④有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易与水反应,产生大量白雾 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
请按要求填写下列问题:
(1)仪器A是一种冷凝管,其作用是可以使甲容器中挥发出的一些物质冷凝,再回到甲容器中。仪器A冷却水的进口为________(填“a”或“b”)。仪器B的作用是________________。
(2)装置丙的作用为除去Cl2中混有的部分HCl。整套装置中若缺少装置乙,根据已知信息判断能否成功制得硫酰氯?(填写能或者不能)____________________。
(3)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H===H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是________。
(4)尝试写出本实验制取氯气的离子方程式________________________,可以看出被氧化的氯原子和被还原的氯原子的个数比为________。