题目内容
16.铍(Be)与铝的性质相似,已知反应BeCl2+Na2BeO2+2H2O═2NaCl+2Be(OH)2↓能进行完全.据此作出的以下推断中正确的是( )| A. | 常温时,BeCl2溶液的pH>7 | |
| B. | 常温时,Na2BeO2溶液的pH<7 | |
| C. | Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 | |
| D. | BeCl2水溶液的导电性较强,说明BeCl2一定是离子化合物 |
分析 在周期表中Be和Al位于对角线位置,性质相似,由反应BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓可知,BeCl2与Na2BeO2发生互促水解生成Be(OH)2,类似于氯化铝与偏铝酸钠的反应,以此解答该题.
解答 解:A.BeCl2为强酸弱碱盐,水解呈酸性,溶液的pH<7,故A错误;
B.Na2BeO2溶液水解呈碱性,溶液的pH>7,故B错误;
C.Be(OH)2性质类似于氢氧化铝,具有两性,则既能溶于盐酸,又能溶于NaOH溶液,故C正确;
D.根据化合物在熔融状态下能否导电来判断其是否是离子化合物,BeCl2水溶液导电性强,不能说明BeCl2是离子化合物,故D错误;
故选C.
点评 本题考查盐类水解的应用,侧重于学生自学能力的考查,题目难度中等,注意从铝的性质类比分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)?2Z(g),此反应达到平衡的标志是( )
| A. | 容器内X、Y、Z的浓度不随时间变化 | |
| B. | 容器内气体密度不随时间变化 | |
| C. | v (X):v (Y)=l:2 | |
| D. | 单位时间消耗0.1 molX同时生成0.2molZ |
4.某化学兴趣小组用图所示装置制备干燥纯净的氯气,并探究氯气的性质.请回答下列问题:
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;若用200mL10mol•L-1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化氢挥发),则产生氯气的物质的量为小于0.5mol(选填“大于”、“小于”、“等于”).
(2)兴趣小组的同学准备在F中装入FeCl2溶液以验证Cl2的氧化性,则该反应的化学方程式2FeCl2+3Cl2=2FeCl3.
(3)兴趣小组同学一致认为氯气能使湿润的红色布条褪色,但对于使湿润的红色布条褪色的原因看法不一致,为探究原因,特设计下列实验.(已知:Cl2+H2O?HCl+HClO)
(4)兴趣小组的某同学认为整套实验装置还存在一处明显缺陷,该缺陷是缺乏尾气处理装置.
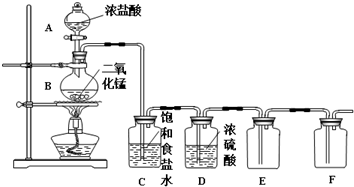
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;若用200mL10mol•L-1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化氢挥发),则产生氯气的物质的量为小于0.5mol(选填“大于”、“小于”、“等于”).
(2)兴趣小组的同学准备在F中装入FeCl2溶液以验证Cl2的氧化性,则该反应的化学方程式2FeCl2+3Cl2=2FeCl3.
(3)兴趣小组同学一致认为氯气能使湿润的红色布条褪色,但对于使湿润的红色布条褪色的原因看法不一致,为探究原因,特设计下列实验.(已知:Cl2+H2O?HCl+HClO)
| 提出假设 | 验证假设 | 得出结论 |
| ①能使红色布条褪色是HCl ②能使红色布条褪色是HClO ③能使红色布条褪色是Cl2(写化学式) | 实验①:把红色布条伸入稀盐酸中,红色布条不褪色. 实验②:E、F分别装入A(填标号),干燥的红色布条不褪色,湿润的红色布条褪色. A.干燥的红色布条、湿润的红色布条 B.湿润的红色布条、干燥的红色布条 | 氯水中的HClO (写化学式)能使湿润的红色布条褪色. |

1.用酒精加热下列各物质,有单质生成的是( )
| A. | 浓HNO3 | B. | NaHCO3 | C. | NH4Cl | D. | Fe(OH)3 |
8.试管中盛有少量白色固体,确认其是铵盐的方法是( )
| A. | 加水,将湿润的红色石蕊试纸放在试管口 | |
| B. | 加氢氧化钠溶液,加热,滴入紫色石蕊试剂 | |
| C. | 加氢氧化钠溶液,加热,滴入酚酞试剂 | |
| D. | 加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口 |
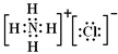 ,氧化钠的电子式
,氧化钠的电子式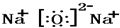 ,CO2的电子式
,CO2的电子式 .
.