��Ŀ����
����Ŀ�����ȷ�Ӧ������һ����Ҫ���ʣ���������;ʮ�ֹ㷺�������ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â����ֽ©�����²����մ���������������ɳ�С�����֪��Al��Al2O3��Fe��Fe2O3���۵㡢�е����������
���� | Al | Al2O3 | Fe | Fe2O3 |
�۵�/�� | 660 | 2 054 | 1 535 | 1 462 |
�е�/�� | 2 467 | 2 980 | 2 750 | - |
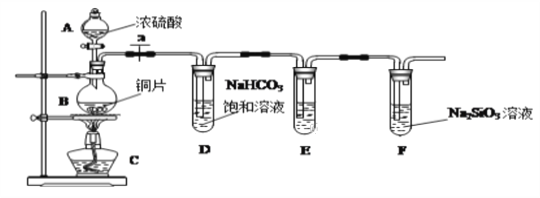
I����1��ijͬѧ�Ʋ⣬���ȷ�Ӧ���õ���������Ӧ�������Ͻ������ǣ��÷�Ӧ�ų�������ʹ���ۻ����������۵�����ͣ���ʱҺ̬���������ۺ��γ������Ͻ�����Ϊ���Ľ����Ƿ������ ______ ���������������������
��2�����һ����ʵ�鷽����֤���������õĿ�״�������к��н���������Ӧ�����ӷ���ʽΪ ______ ��
��3��ʵ�����ܽ��������������Լ��������˵��Լ��� ______ ������ţ���
A��Ũ����B��ϡ���ᡡ������C��ϡ����D������������Һ
��ʵ���о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�ͣ�ijͬѧȡһ������������������һ������ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���6molL-1������������Һ����������������Һ�������mL��������ij��������ʵ�����mol���Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
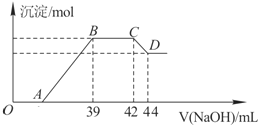
��1�������⣬��д���������������ϡ�����ᷴӦ�����ӷ���ʽ�� ______
��2����BC�Σ����������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽΪ ______ ��
��3������������Ԫ�ص����ʵ���Ϊ ______ mol��
��4��B���Ӧ�ij��������ʵ���Ϊ ______ mol��A���Ӧ������������Һ�����Ϊ ______ mL��
���𰸡� ���� 2Al+2OH-+2H2O=2AlO2-+3H2�� B 8Fe+30H++3NO3-=8Fe3++3NH4++9H2O NH4++OH-=NH3H2O 0.012 0.048 15
����������1�������۵�����ͣ���������Һ̬��һ�������ʢ��ɳ�ӵ��������γɺϽ��������ȷ�Ӧ���õ���������Ӧ�������Ͻ𣬹ʽ��ͺ���������NaOH��Һ��Ӧ�������壬��Ӧ�����ӷ���ʽΪ2Al+2OH��+2H2O=2AlO2��+3H2������3��A��Ũ������ʹ�������ۻ�������ʹ�Ͻ��ܽ⣬��A����B�����ý�����ϡ���ᷴӦ����������ܽ���ϡ�����У���B��ȷ��C��ϡ�����������Ӧ������Ⱦ�����壬�������ѡ��C����D��������NaOH��Һ��Ӧ�����ܽ�������ȫ���ܽ⣬��D����ѡB����1����������ϡ���ᷴӦ������������������ƶϳ���ԭ����ӦΪNH4�������������ϡ�����ᷴӦ�����ӷ���ʽΪ8Fe+30H��+3NO3���T8 Fe3��+3NH4��+9 H2O����2��BC�γ���������û�з����仯��ΪNH4NO3��NaOH��Ӧ�����ӷ���ʽΪNH4��+OH���TNH3��H2O������3��CD�η����ķ�Ӧ��Al��OH��3 +OH��=AlO2��+2H2O��n��NaOH��=0.002L��6mol��L��1=0.012mol����n��Al��OH��3��=0.012mol��������������Ԫ�ص����ʵ���Ϊ0.012mol����4����8Fe+30H��+3NO3���T8 Fe3��+3NH4��+9 H2O��8Al+30H��+3NO3���T8 Al3��+3NH4��+9 H2O��NH4��+OH���TNH3��H2O�ɵù�ϵʽ8��Fe��Al����3NH4����3OH����BC�����ĵ�OH�������ʵ���Ϊ6mol��L-1����42-39����10-3L=0.018mol����Fe��Al�����ʵ���֮��Ϊ0.018mol��8/3=0.048mol������B���Ӧ�ij���Fe��OH��3��Al��OH��3�����ʵ���Ϊ0.048mol��AB�����ĵ�����������Һ���ʵ���Ϊ0.048mol��3=0.144mol��AB�����ĵ��������Ƶ����Ϊ0.144mol/6mol��L��1=0.024L=24ml������A���Ӧ������������Һ�����Ϊ39-24=15��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ�����������й���;�����ʵĶ�Ӧ��ϵ������ǣ� ��
���� | ��; | ���� | |
A | С�մ� | ���ڱ��Ƹ�� | С�մ�����Ӧ |
B | ������ | ����ұ���ѡ�ﯵȽ��� | ��������ǿ��ԭ�� |
C | �������� | ������Ư�ոѡ�֯�� | SO2�ܸ����е���ɫ���ʽ�� |
D | ���� | ����ʳƷ�е������� | Fe���л�ԭ�� |
A.AB.BC.CD.D
����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ�����о�NO2��NO��CO��S02�ȴ�����Ⱦ���ˮ��Ⱦ��Ĵ����Խ��������й�������Ҫ���塣
(1)��֪�� ��NO2+CO![]() CO2+NO�÷�Ӧ��ƽ�ⳣ��ΪK1(��ͬ)��ÿ1mol�������ʷֽ�Ϊ��̬��̬ԭ�����յ������ֱ�Ϊ
CO2+NO�÷�Ӧ��ƽ�ⳣ��ΪK1(��ͬ)��ÿ1mol�������ʷֽ�Ϊ��̬��̬ԭ�����յ������ֱ�Ϊ
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
��N2(g)+O2(g) ![]() 2NO(g) ��H=+179.5kJ/mol K2
2NO(g) ��H=+179.5kJ/mol K2
��2NO(g)+O2(g)![]() 2NO2(g) ��H=-112.3kJ/mol K3
2NO2(g) ��H=-112.3kJ/mol K3
д��NO��CO��Ӧ��������Ⱦ������Ȼ�ѧ����ʽ____________________________________�����Ȼ�ѧ����ʽ��ƽ�ⳣ��K=_________(��K1��K2��K3��ʾ)��
(2)������ɱ�ĺ�ѹ(p��)�ܱ������г���1molCO2 ��������̼�����䷢����Ӧ�� C(s)+ CO2(g)![]() 2CO(g) ��H>0��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
2CO(g) ��H>0��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
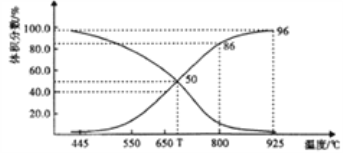
��T��ʱ����������������ϡ�����壬v(��)___v(��)(�>����<����=")��ƽ��______�ƶ�(���������������ͬ)��������������CO2 ��CO��ƽ��________�ƶ���
��CO�������Ϊ40%ʱ��CO2 ��ת����Ϊ_______��
����֪�������ѹ(p��)=������ѹ�������������ƽ���ѹ����ƽ��Ũ�ȱ�ʾƽ��Kp�����ı���ʽΪ__________��925��ʱ��Kp=______(�ú�p���Ĵ���ʽ��ʾ)��
(3)ֱ���ŷź�SO2 ���������γ����꣬Σ������������NaOH���գ����ú������(H2SO3��HSO3-��SO32-)�����ڷ�Ӧ�����Һ�У����ǵ����ʵ�������X(i)����ҺpH�Ĺ�ϵ��ͼ��ʾ��

������0.1mol/LNaOH ��Ӧ�����Һ�������Һ��pH=8ʱ����Һ�и�����Ũ���ɴ�С��˳����______________��
����pH=5��NaHSO3��Һ�еμ�һ��Ũ�ȵ�CaCl2 ��Һ����Һ�г��ֻ��ǣ�pH��Ϊ2���û�ѧƽ���ƶ�ԭ��������ҺpH���͵�ԭ��_______________________________________________��