题目内容
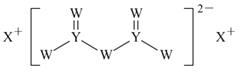
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.化合物M中W不都满足8电子稳定结构
【答案】B
【解析】
短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,为钠Na;由W、X、Y三种元素形成的化合物M的结构分析,Y形成四个共价键,说明其为Si;Y的原子序数是Z的最外层电子数的2倍,则Z为Cl;W的核外电子数与X、Z的最外层电子数之和相等,为O;依此答题。
经分析,X为Na,Y为Si,Z为Cl,W为O,则:
A.O、Si、Cl三种元素非金属性最强的为Cl,A错误;
B.单质Si为原子晶体,单质Na是金属晶体,单质Si的熔点高于单质Na,B正确;
C.O的非金属性比Si强,所以O的氢化物的稳定性比Si的氢化物强,C错误;
D.化合物M中O都满足8电子结构,D错误;
故选B。

练习册系列答案
相关题目
【题目】下列有关仪器的名称、图形、用途与使用操作的叙述均正确的是( )
选项 | A | B | C | D |
名称 | 250 mL容量瓶 | 分液漏斗 | 酸式滴定管 | 冷凝管 |
图形 |
|
|
|
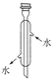
|
用途与使用操作 | 配制1.0 mol·L-1NaCl溶液,定容时俯视刻度,则配得的溶液浓度小于1.0 mol·L-1 | 用甘油萃取碘水中的碘,分液时,碘层需从上口放出 | 可用于量取10.00mL 新制氯水溶液 | 蒸馏实验中将蒸气冷凝为液体 |
A.AB.BC.CD.D