��Ŀ����
����Ŀ����ʹ������к͵ζ����ⶨ�����������������g/100mL����
��ʵ�鲽�裺
��1������ʽ�ζ���ȡ����������Һ20.00mL����ƿ�У������еμ�2��___��ָʾ����
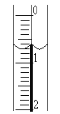
��2����ȡʢװ0.1000mol/LNaOH��Һ�ļ�ʽ�ζ��ܵij�ʼ���������Һ��λ����ͼ��ʾ�����ʱ�Ķ���Ϊ____mL��
��3���ζ�����___ʱ��ֹͣ�ζ�������¼NaOH��Һ���ն������ظ��ζ�3�Ρ�
��ʵ���¼
�ζ����� ʵ�����ݣ�mL�� | 1 | 2 | 3 | 4 |
V(��Ʒ) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)�����ģ� | 15.95 | 15.00 | 15.05 | 14.95 |
�����ݴ��������ۣ�
��4����ͬѧ�ڴ�������ʱ����ã�
ƽ�����ĵ�NaOH��Һ�����V=(15.95+15.00+15.05+14.95)/4mL = 15.24mL��
ָ�����ļ���IJ�����֮����___������ȷ���ݴ������ɵ�c(��������)=___mol/L��
���𰸡���̪ 0.70 ��Һ����ɫ��Ϊ�ۺ�ɫ���Ұ�����ڲ���ɫ ��1���������ϴ�Ӧ���� 0.075
��������
��1����Һ���ᵽ���ɫ����ɫ��Ϊdz��ɫ��
��2���ζ�����Һ����°���λ��0.70mL����
��3�����������һ��NaOH��Һʱ����Һ����ɫ��Ϊ�ۺ�ɫ���Ұ�����ڲ���ɫ����ζ��ﵽ�յ㡣
��4�����ݱ������ݣ���1��ʵ������̫��Ӧ�������ã�����c1=c2��V2/V1���㡣
��1����̪�������ᣬ��ҺΪ��ɫ�����������һ��NaOH��Һʱ����Һ�Լ��ԣ���Һ��dz��ɫ���÷�̪��ָʾ��ʱ����Һ��ɫ�仯��dz������ڹ۲죻
��2���ζ�����Һ����°���λ��0.70mL���������Ϊ0.70mL��
��3�����������һ��NaOH��Һʱ����Һ����ɫ��Ϊ�ۺ�ɫ���Ұ�����ڲ���ɫ����ζ��ﵽ�յ㡣
��4�����ݱ������ݣ���1��ʵ������̫��Ӧ�������ã�V=(15.00+15.05+14.95)/4=15.00mL������c1=c2��V2/V1=0.1000mol/L��15.00mL/20.00mL=0.075mol/L��

 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�