题目内容
【题目】已知 As元素的部分信息如图所示,下列说法不正确的是

A. H3AsO4和H3PO4都能与NaOH溶液反应生成相应的盐
B. 热稳定性:AsH3、H2S、HCl逐渐增强
C. As的一种核素表示为![]() ,中子数为40
,中子数为40
D. 原子半径由大到小的顺序:As、Cl、Si
【答案】D
【解析】
A. H3AsO4和H3PO4都为多元弱酸,均能与NaOH溶液反应生成相应的盐,选项A正确;B. 元素非金属性越强,简单气态氢化物的稳定性越强,非金属性As<S<Cl,故热稳定性:AsH3、H2S、HCl逐渐增强,选项B正确;C. As的一种核素表示为![]() ,中子数为73-33=40,选项C正确;D. 同周期元素从左到右原子半径逐渐减小,同主族元素从上而下原子半径逐渐增大,故原子半径由大到小的顺序:As、Si、Cl,选项D不正确。答案选D。
,中子数为73-33=40,选项C正确;D. 同周期元素从左到右原子半径逐渐减小,同主族元素从上而下原子半径逐渐增大,故原子半径由大到小的顺序:As、Si、Cl,选项D不正确。答案选D。

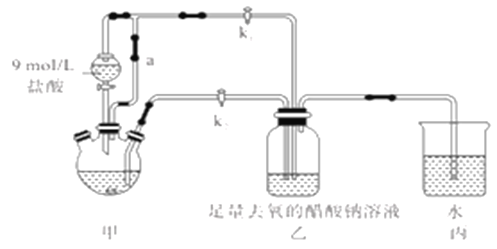
【题目】氯气可用于制取漂白剂和自来水消毒。
(1)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是________(填写化学式)。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为______________________。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5 mL市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20 mL分别加入3个洁净的小烧杯中;
步骤3:用H2SO4溶液将3个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 | 溶液的pH | 现象 |
a | 10 | 10 min后,红纸基本不褪色;4 h后红纸褪色 |
b | 7 | 10 min后,红纸颜色变浅;4 h后红纸褪色 |
c | 4 | 10 min后,红纸颜色变得更浅;4 h后红纸褪色 |
已知,溶液中Cl2、HClO和ClO-物质的量分数(α)随溶液pH变化的关系如下图所示:
![]()

①由实验现象可获得以下结论:溶液的pH在4~10范围内,pH越大,红纸褪色________。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是________。
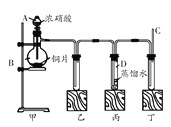
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如ClO2气体就是一种新型高效含氯消毒剂。
①一种制备ClO2的方法是用SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为________。
②另一种制备ClO2的方法是用NaClO3与盐酸反应,同时有Cl2生成,产物中Cl2体积约占1/3,每生成0.5 mol ClO2,转移________mol e-。