题目内容
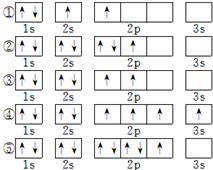
A、B、C、D、E、F为原子序数依次增大的短周期主族元素.A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F.
(1)写出B的基态原子的核外电子排布式______.
(2)A、C形成的最简单分子极易溶于水,其主要原因是______;与该最简单分子互为等电子体的阳离子为______.
(3)比较E、F的第一电离能:E______F(选填“>”或“<”,“=”).
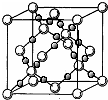
(4)BD2在高温高压下所形成的晶胞如右图所示.该晶体的类型属于______(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为______.
(5)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在______.
a.共价键b.非极性键c.配位键d.σ键e.π键.
(1)写出B的基态原子的核外电子排布式______.
(2)A、C形成的最简单分子极易溶于水,其主要原因是______;与该最简单分子互为等电子体的阳离子为______.
(3)比较E、F的第一电离能:E______F(选填“>”或“<”,“=”).
(4)BD2在高温高压下所形成的晶胞如右图所示.该晶体的类型属于______(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为______.
(5)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在______.
a.共价键b.非极性键c.配位键d.σ键e.π键.

(1)B元素为碳元素,根据核外电子排布规律,C元素的基态原子的核外电子排布式为:1s22s22p2,故答案为:1s22s22p2;
(2)A、C形成的最简单分子是NH3分子,是一种极性分子,极易溶于水的原因主要有:
①根据相似相溶原理,氨气易溶于极性溶剂水中;
②氨气分子在水中易与水分子形成氢键,增大了氨气的溶解性;
③部分氨气与水反应,降低了NH3浓度,使溶解量增大;
所谓等电子体是指一类分子或离子,组成它们的原子数相同,而且所含的价层电子数相同,则它们互称为等电子体.与氨气分子互为等电子体的阳离子为H3O+,
故答案为:NH3与H2O间能形成氢键;H3O+;
(3)电离能可以衡量元素的原子失去一个电子的难易程度(可近似理解为金属性).第一电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,原子越难失去一个电子.存在的规律为:
①随着核电荷数的递增,元素的第一电离能呈现周期性变化;②总体上金属元素第一电离能较小非金属元素第一电离能较大; ③同周期元素第一电离能从左到右有增大的趋势.所以同一周期第一电离能最小的是碱金属元素,最大的是稀有气体元素;
④同一周期内元素的第一电离能在总体增大的趋势中有些曲折.当外围电子在能量相等的轨道上形成全空(p0,d0,fo)、半满(p3,d5,f7)或全满(p6,d10,f14)结构时,原子的能量较低,元素的第一电离能较大.特例是第二主族的第一电离能大于第三主族,第五主族的第一电离能大于第六主族; ⑤同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,第一电离能由大变小,元素的金属性逐渐增强,则镁原子结构中各亚层均处于全满状态,所以镁比铝的第一电离能反常高,
故答案为:>;
(4)根据BD2即CO2在高温高压下所形成的晶胞晶胞结构可知,该晶体为原子晶体,晶胞内白球为C原子,黑球为O原子,每个晶胞中含碳原子为8×
+6×
+4=8,含氧原子为16,所以碳原子和氧原子微粒数之比为1:2,根据晶胞中碳原子和氧原子的结构可知,碳原子的杂化方式为SP3杂化,故答案为:原子;sp3;
(5)光谱证实单质AI与强碱性溶液反应有[AI(OH)4]-生成,可看作其中铝原子和三个羟基形成三对共用电子对,形成三个极性共价键,形成AI(OH)3;AI(OH)3溶解在强碱中,和OH-形成[AI(OH)4]-,利用的是铝原子的空轨道和氢氧根离子的孤对电子形成的配位键;
由两个相同或不相同的原子轨道沿轨道对称轴方向相互重叠而形成的共价键,叫做σ键,所以[AI(OH)4]-中也形成了σ键.
故答案为:acd.
(2)A、C形成的最简单分子是NH3分子,是一种极性分子,极易溶于水的原因主要有:
①根据相似相溶原理,氨气易溶于极性溶剂水中;
②氨气分子在水中易与水分子形成氢键,增大了氨气的溶解性;
③部分氨气与水反应,降低了NH3浓度,使溶解量增大;
所谓等电子体是指一类分子或离子,组成它们的原子数相同,而且所含的价层电子数相同,则它们互称为等电子体.与氨气分子互为等电子体的阳离子为H3O+,
故答案为:NH3与H2O间能形成氢键;H3O+;
(3)电离能可以衡量元素的原子失去一个电子的难易程度(可近似理解为金属性).第一电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,原子越难失去一个电子.存在的规律为:
①随着核电荷数的递增,元素的第一电离能呈现周期性变化;②总体上金属元素第一电离能较小非金属元素第一电离能较大; ③同周期元素第一电离能从左到右有增大的趋势.所以同一周期第一电离能最小的是碱金属元素,最大的是稀有气体元素;
④同一周期内元素的第一电离能在总体增大的趋势中有些曲折.当外围电子在能量相等的轨道上形成全空(p0,d0,fo)、半满(p3,d5,f7)或全满(p6,d10,f14)结构时,原子的能量较低,元素的第一电离能较大.特例是第二主族的第一电离能大于第三主族,第五主族的第一电离能大于第六主族; ⑤同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,第一电离能由大变小,元素的金属性逐渐增强,则镁原子结构中各亚层均处于全满状态,所以镁比铝的第一电离能反常高,
故答案为:>;
(4)根据BD2即CO2在高温高压下所形成的晶胞晶胞结构可知,该晶体为原子晶体,晶胞内白球为C原子,黑球为O原子,每个晶胞中含碳原子为8×
| 1 |
| 8 |
| 1 |
| 2 |
(5)光谱证实单质AI与强碱性溶液反应有[AI(OH)4]-生成,可看作其中铝原子和三个羟基形成三对共用电子对,形成三个极性共价键,形成AI(OH)3;AI(OH)3溶解在强碱中,和OH-形成[AI(OH)4]-,利用的是铝原子的空轨道和氢氧根离子的孤对电子形成的配位键;
由两个相同或不相同的原子轨道沿轨道对称轴方向相互重叠而形成的共价键,叫做σ键,所以[AI(OH)4]-中也形成了σ键.
故答案为:acd.

练习册系列答案
相关题目
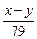
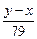
 (1)氨催化氧化的化学方程式为 :
(1)氨催化氧化的化学方程式为 :