题目内容
4.a的金属活动性比氢强,b为碳棒,关于下列装置的说法中不正确的是( )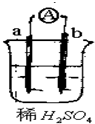
| A. | a发生氧化反应,b发生还原反应 | B. | 碳棒上有气体逸出 | ||
| C. | 导线上有电流,电流方向从a→b | D. | 反应后a极质量减小 |
分析 根据装置没有电源,则构成原电池装置,又a在金属活动性顺序表中排在氢之前,b为碳棒,则a为负极本身失电子发生氧化反应,b为正极溶液中的氢离子得电子发生还原反应,电子从负极流向正极,据此分析.
解答 解:A.a为负极本身失电子发生氧化反应,b为正极溶液中的氢离子得电子发生还原反应,故A正确;
B、b为正极溶液中的氢离子得电子发生还原反应,所以碳棒上有气体逸出,故B正确;
C、电流从正极流向负极,即从b→a,故C错误;
D、根据装置没有电源,则构成原电池装置,又a在金属活动性顺序表中排在氢之前,b为碳棒,则a为负极本身失电子发生氧化反应,所以a极质量减小,故D正确;
故选C.
点评 本题考查原电池原理,明确正负极上得失电子是解本题关键,难度不大,注意对基础知识的归纳整理.

练习册系列答案
相关题目
12.强酸和强碱在稀溶液中的中和热可表示为:
H+(aq)+OH-(aq)=H2O(l);△H=-57.3k kJ•mol-1,
又知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H=-Q1kJ•mol-1,
$\frac{1}{2}$H2SO4(浓)+$\frac{1}{2}$Ba(OH)2(aq)=$\frac{1}{2}$BaSO4(aq)+H2O(l);△H=-Q2 kJ•mol-1
HNO3(aq)+KOH(aq)═KNO3(aq)+H2O(l);△H=-Q3 kJ•mol-1,
上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系是( )
H+(aq)+OH-(aq)=H2O(l);△H=-57.3k kJ•mol-1,
又知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H=-Q1kJ•mol-1,
$\frac{1}{2}$H2SO4(浓)+$\frac{1}{2}$Ba(OH)2(aq)=$\frac{1}{2}$BaSO4(aq)+H2O(l);△H=-Q2 kJ•mol-1
HNO3(aq)+KOH(aq)═KNO3(aq)+H2O(l);△H=-Q3 kJ•mol-1,
上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系是( )
| A. | Q2>Q3>Q1 | B. | Q2>Q1>Q3 | C. | Q1=Q2=Q3 | D. | Q2=Q3>Q1 |
15.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体不是纯净物的是( )
| A. | 向红褐色的Fe(OH)3固体中加入过量盐酸 | |
| B. | 等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液 | |
| C. | 等物质的量的NaHCO3与Na2O2固体 | |
| D. | 向NaBr溶液中通入过量氯气 |
12.下列离子方程式正确的是( )
| A. | Ca(HCO3)2溶液中加入过量NaOH溶液Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| B. | SO2通入溴水中SO2+Br2+2H2O═4H++2Br-+SO42- | |
| C. | 泡沫灭火器原理:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| D. | FeO与稀HNO3反应FeO+2H+═Fe2++H2O |
9.下列有关化学与生活的说法不正确的是( )
| A. | 采用原煤脱硫技术,可减少燃煤产生的SO2 | |
| B. | 晶体硅可以制作太阳能电池板 | |
| C. | 自来水厂可用氯气来杀菌消毒,因此氯气无毒 | |
| D. | 分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液 |
16.反应C(s)+H2O(g)?CO(g)+H2(g)在一密闭容器中进行并达平衡.下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加C(s)的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 升高体系温度 | |
| D. | 保持压强不变,充入氩气使容器体积增大 |
13.对于化学反应:C+4HNO3═CO2+4NO2+2H2O,下列说法正确的是( )
| A. | HNO3在反应中表现氧化性 | |
| B. | C在反应中被还原 | |
| C. | HNO3在反应中失去电子 | |
| D. | 1 mol 氧化剂在反应中得到4 mol电子 |
14.下列表示物质或微粒的化学用语正确的是( )
| A. | Mg 2+的结构示意图: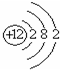 | B. | NH3分子的电子式: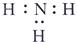 | ||
| C. | H2S的结构式:H-S-H | D. | CH4分子的比例模型: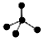 |