题目内容
(12分)手持技术又称掌上技术,是由数据采集器、传感器和配套的软件成
的定量采集各种常见数据并能与计算机连接的实验技术系统。某研究小组利用手持技术,获得8.34gFeS04·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
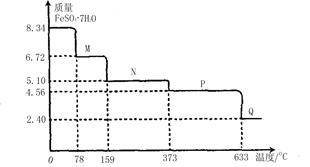
请回答下列问题:
(1)试确定78℃时固体物质M的化学式: 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成且两种气体的组成元素相同,摩尔质量相差16,写出该反应的化学方程式 。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
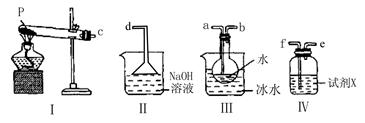
①试剂X的名称是 。
②按气流方向连接各仪器,用字母表示接口的连接顺序:c 。
③充分反应后,利用装置Ⅲ中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。第三步:继续烘干、冷却并称量直至连续两次 称量的质量差不超过0.1g为止。若最终得到沉淀的质量为Wg,则已分解的P的质量为 (填计算式)。
④上述测得P的质量比实际分解质量要小,原因是 。
的定量采集各种常见数据并能与计算机连接的实验技术系统。某研究小组利用手持技术,获得8.34gFeS04·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。

请回答下列问题:
(1)试确定78℃时固体物质M的化学式: 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成且两种气体的组成元素相同,摩尔质量相差16,写出该反应的化学方程式 。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。

①试剂X的名称是 。
②按气流方向连接各仪器,用字母表示接口的连接顺序:c 。
③充分反应后,利用装置Ⅲ中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。第三步:继续烘干、冷却并称量直至连续两次 称量的质量差不超过0.1g为止。若最终得到沉淀的质量为Wg,则已分解的P的质量为 (填计算式)。
④上述测得P的质量比实际分解质量要小,原因是 。
(1)FeS04·4H20 (2)2FeSO4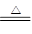 Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
(3)①品红溶液或溴水或酸性高锰酸钾溶液
②a b
b f
f e
e d ③
d ③
④由于生成的三氧化硫并没有完全被吸收,导致生成的硫酸钡质量减少
 Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑(3)①品红溶液或溴水或酸性高锰酸钾溶液
②a
 b
b f
f e
e d ③
d ③
④由于生成的三氧化硫并没有完全被吸收,导致生成的硫酸钡质量减少
试题分析:(1)8.34gFeS04·7H20的物质的量是8.34g÷278g/mol=0.03mol,78℃是固体质量减少了8.34g-6.72g=1.62g,即相当于水的物质的量是1.62g÷18g/mol=0.09mol,所以固体中含有的结晶水是0.03mol×7-0.09mol=0.12mol,则化合物中含有的水分子个数是0.12mol÷0.03mol=4,则化学式是FeS04·4H20。
(2)固体加热到373℃时固体质量减少了8.34g-4.56g=3.78g,即相当于水的物质的量是3.78g÷18g/mol=0.21mol,这说明此时水已经完全失去。又因为两种气体的组成元素相同,摩尔质量相差16,所以该物质是二氧化硫和三氧化硫,因此反应的化学方程式是2FeSO4
 Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。(3)①二氧化硫具有漂白性和还原性,所以检验二氧化硫可以用品红溶液或溴水或酸性高锰酸钾溶液。
②三氧化硫溶于水生成硫酸,所以首先要通过冷却水得到三氧化硫,又因为二氧化硫是大气污染物,需要尾气处理,所以正确的顺序是c
 a
a b
b f
f e
e d。
d。③根据题意最终得到的白色沉淀是硫酸钡,由于生成的硫酸来自于三氧化硫,所以根据S原子守恒可知,分解的硫酸亚铁的质量是
 。
。④由于生成的三氧化硫并没有完全被吸收,导致生成的硫酸钡质量减少,所以测得P的质量比实际分解质量要小。2的检验、三氧化硫的分离等
点评:固体是高考中的常见题型,属于较难的实验题。试题既有定性的分析,也有定量的计算,学生不易得分。本题用图表表述化学过程或呈现背景信息是化学常用的表达方式。图表往往拥有较大的信息存储量,能够很全面地考查学生分析、比较、概括、归纳问题的能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 Cu(OH)2+2H+反应平衡常数 。
Cu(OH)2+2H+反应平衡常数 。
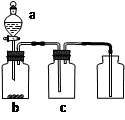
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):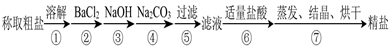
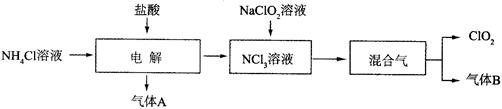
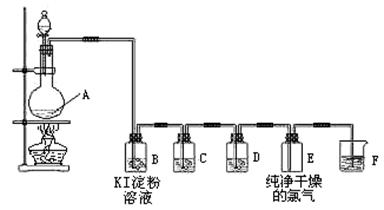
 MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是 ;
MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是 ;