题目内容
3.能正确表示下列化学反应的离子方程式的是( )| A. | 氢氧化钡溶液与硫酸的反应OH-+H+=H2O | |
| B. | 铝粉投入到NaOH溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
分析 A.漏掉了钡离子与硫酸根离子反应生成硫酸钡的反应;
B.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气;
C.离子方程式两边正电荷不相等,不满足电荷守恒;
D.氨水为弱碱,一水合氨不能拆开,需要保留分子式.
解答 解:A.稀硫酸和Ba(OH)2溶液生成的硫酸钡和水,正确的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A错误;
B.铝粉投入到NaOH溶液中,二者反应生成偏铝酸钠和氢气,反应的离子方程为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故B正确;
C.铜片插入硝酸银溶液中,反应生成铜离子和银,正确的离子方程式为:Cu+2Ag+=Cu2++2Ag,故C错误;
D.氯化铝与氨水反应生成氢氧化铝沉淀,一水合氨不能拆开,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
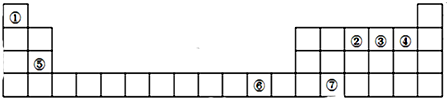
13.如图是元素周期表的一部分,下列说法中,正确的是( )


| A. | 元素①位于第二周期第ⅣA族 | B. | 气态氢化物的稳定性:⑤>③ | ||
| C. | 元素的最高正化合价:④=② | D. | 最高价氧化物对应水化物酸性:⑤>④ |
11.下列说法中不正确的是( )
| A. | 共价化合物中一定不含有离子键,离子化合物中可能含有共价键 | |
| B. | 一定条件下,将1 mol N2与3 mol H2充入密闭容器中充分反应可生成2 mol NH3 | |
| C. | 充电电池的化学反应原理是氧化还原反应 | |
| D. | Na2O和Na2O2晶体中阳离子与阴离子个数比均为2:1 |
18.等质量的铜片在酒精灯上加热后,分别插入下列液体中,放置片刻后取出,铜片质量增加的是( )
| A. | 盐酸 | B. | 无水乙醇 | C. | 稀硝酸 | D. | NaOH溶液 |
15.高温下,某反应达到平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| A. | 该反应的化学方程式为CO+H2O$\frac{\underline{\;催化剂\;}}{高温}$CO2+H2 | |
| B. | 该反应的焓变为正值 | |
| C. | 恒温恒容下,充入氮气,平衡右移 | |
| D. | 升高温度,逆反应速率减小 |
12.某密闭容器中充入等物质的量的气体A和B,一定温度下发生如下反应:A(g)+xB(g)═2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示.下列说法中正确的是( )


| A. | 反应方程式中的x=1,30min时改变条件后,A的转化率将变减小 | |
| B. | 前30 min内 A的反应速率为0.05 mol/(L•min) | |
| C. | 20至40 min内表示处于平衡状态,该反应为放热反应 | |
| D. | 30 min时改变的条件是加入负催化剂,40 min时改变的条件是升高温度 |
13.光具有能量,能影响很多反应.下列反应中,受光照影响显著的是( )
| A. | 铁与氯气反应 | B. | 次氯酸的分解 | ||
| C. | 乙醇与乙酸的酯化反应 | D. | 甲烷与氧气的反应 |