题目内容
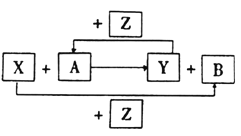
【题目】中国第二化工设计院提出,用间接电化学法对大气污染物NO进行无害化处理,其原理示意如图(质子膜允许H+和H2O通过),下列相关判断正确的是
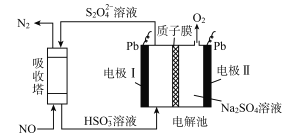
A. 电极I为阴极,电极反应式为2H2O+2e-=2OH-+H2
B. 电解池中质子从电极I向电极Ⅱ作定向移动
C. 吸收塔中的反应为2NO+2S2O32-+H2O=N2+4HSO3-
D. 每处理1 mol NO电解池质量减少16g
【答案】C
【解析】A. 电极I为阴极,阴极上是HSO3-获得电子生成S2O42-,酸性条件下还生成水,电极反应式为:2HSO3-+2H++2e-=S2O42-+2H2O,故A错误;B. 电解池中质子从电极Ⅱ向电极I作定向移动,故B错误;C. 吸收池中S2O42-与NO反应生成N2与HSO3-,反应离子方程式为:吸收塔中的反应为2NO+ 2S2O32-+H2O=N2+4HSO3-,故C正确;D、电解池中发生的反应:4HSO3-=2H2O+O2+2S2O42-,结合吸收塔中的反应:2NO+ 2S2O32-+H2O=N2+4HSO3-,得关系式:2NO~O2~4H+,每处理1 mol NO电解池质量减少16 gO2和2gH+,共18g,故D错误;故选C。

【题目】某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平离子方程式(将化学计量数填于空白处)____I-+____IO3—+____H+ =____I2+____H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的化学方程式是:____________________________。
②某学生设计回收四氯化碳的操作为:a.加入适量Na2SO3稀溶液; b.分离出下层液体;c.将碘的四氯化碳溶液置于分液漏斗中; d.将分液漏斗充分振荡后静置。其中分液漏斗使用前须进行的操作是_______,上述操作正确的顺序是:_______(填序号)
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:a.准确称取ag食盐,加适量蒸馏水使其完全溶解;b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;c.以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是_______________________。
②b中反应所消耗的KI的物质的量是____________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含a的代数式表示)_____mg/kg。
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 某溶液中加入盐酸酸化的 | 白色沉淀 | 溶液中一定含有 |
B | 用激光笔照射鸡蛋白溶液 | 有丁达尔效应 | 鸡蛋白溶液属于胶体 |
C | 某气体通入酸性 | 紫色褪去 | 该气体一定是 |
D | 用铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 溶液中无 |
A. A B. B C. C D. D