题目内容
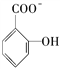
【题目】氯化苄(C6H5CH2Cl)为无色液体,是一种重要的有机化工原料。现在实验室模拟工业上用甲苯与干燥氯气在光照条件下加热反应合成氯化苄、分离出氯化苄并检验样品的纯度,其装置(夹持装置略去)如图所示:
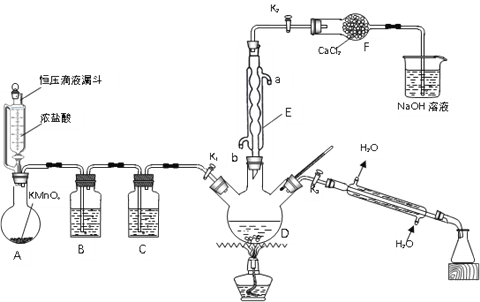
回答下列问题:
(1)仪器E的名称是______;其作用是______;其进水口为______(填“a”或“b”)。
(2)装置B中的溶液为______;装置F的作用是______。
(3)用恒压滴液漏斗代替分液漏斗的优点是______。
(4)装置A中反应的离子方程式为______。
(5)反应结束后,关闭K1和K2,打开K3,加热三颈烧瓶,分馏出氯化苄,应选择温度范围为______℃。
物质 | 溶解性 | 熔点(℃) | 沸点(℃) |
甲苯 | 极微溶于水,能与乙醇、乙醚等混溶 | -94.9 | 110 |
氯化苄 | 微溶于水,易溶于苯、甲苯等有机溶剂 | -39 | 178.8 |
二氯化苄 | 不溶于水,溶于乙醇、乙醚 | -16 | 205 |
三氯化苄 | 不溶于水,溶于乙醇、乙醚和苯 | -7 | 220 |
(6)检测氯化苄样品的纯度:
①称取13.00g样品于烧杯中,加入50.00mL 4 molL-1 NaOH水溶液,水浴加热1小时,冷却后加入35.00mL 40% HNO3,再将全部溶液转移到容量瓶中配成100mL溶液。取20.00mL溶液于试管中,加入足量的AgNO3溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为______%(结果保留小数点后1位)。
②实际测量结果可能偏高,原因是______。
【答案】 球形冷凝管 导出Cl2、HCl气体,冷凝回流甲苯 b 饱和食盐水 防止水蒸气进入装置 使漏斗与烧瓶内压强一致,液体顺利流下 2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O 178.8-205 97. 3 样品混有二氯化苄、三氯化苄等杂质
【解析】分析:A装置中产生氯气,利用B和C装置分别除去氯化氢和水蒸气,干燥后的氯气与甲苯在装置D中反应生成氯化苄,多余的氯气利用氢氧化钠溶液吸收。通过蒸馏装置分离出氯化苄,据此解答。
详解:(1)根据仪器构造可知仪器E的名称是球形冷凝管,其作用是导出Cl2、HCl气体,冷凝回流甲苯;冷却时才有逆向冷却,则其进水口为b。
(2)生成的氯气中含有氯化氢,则装置B中的溶液为饱和食盐水,用来除去氯化氢;装置F中的无水氯化钙是干燥剂,其作用是防止水蒸气进入装置。
(3)恒压滴液漏斗可以保持内外压强相等,因此用恒压滴液漏斗代替分液漏斗的优点是使漏斗与烧瓶内压强一致,液体顺利流下。
(4)装置A中制备氯气,反应的离子方程式为2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O。
(5)根据表中数据可知氯化苄的沸点是178.8℃,因此分馏出氯化苄应选择温度范围为178.8~205℃。
(6)①2.87g固体是氯化银,物质的量是2.87g÷143.5g/mol=0.02mol,因此根据氯原子守恒可知氯化苄的物质的量是0.02mol×100mL/20mL=0.1mol,质量是0.1mol×126.5g/mol=12.65g,则该样品的纯度为12.65g/13.00g×100%=97.3%;
②由于样品混有二氯化苄、三氯化苄等杂质,因此实际测量结果可能偏高。

【题目】锗是一种重要的半导体材料。工业上用精硫锗矿(主要成分为GeS2,杂质不反应)制取Ge,其工艺流程如图所示:

回答下列问题:
(1)开始将精硫锗矿粉碎的目的是______。
(2)高温焙烧精硫锗矿的化学方程式为______。
(3)热还原真空挥发炉内反应的化学方程式为______。
(4)在沉锗过程中,当温度为90℃,pH为14时,加料量(CaCl2/Ge质量比)对沉锗的影响如表所示,选择最佳加料量为______(填“10-15”“15-20”或“20-25”),理由是______。
编号 | 加料量(CaCl2/Ge) | 母液体积 (mL) | 过滤后液含锗(mg/L) | 过滤后液 pH | 锗沉淀率(%) |
1 | 10 | 500 | 76 | 8 | 93.67 |
2 | 15 | 500 | 20 | 8 | 98.15 |
3 | 20 | 500 | 2 | 11 | 99.78 |
4 | 25 | 500 | 1.5 | 12 | 99.85 |
(5)某温度时,沉锗得到的CaGeO3在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是______。

a.n点与p点对应的Ksp相等
b.通过蒸发可以使溶液由q点变到p点
c.q点无CaGeO3沉淀生成
d.加入Na2GeO3可以使溶液由n点变到m点
(6)CaGeO3与强酸反应可得到H2GeO3。0.l molL-1的NaHGeO3溶液pH_____(填“>”“=”或“<”)7,判断理由是______(通过计算比较)。(25℃时,H2GeO3的Ka1=1.7×10-9,Ka2=1.9×10-13。)