题目内容
17.一个体重50kg的健康人含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在.Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4).服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收.(1)“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话指出,维生素C在这个反应中作还原剂,具有还原 性.
(2)已知下列反应在一定条件下发生:

在以上的反应中,Fe2+实际上起着催化剂的作用.
分析 (1)维生素C可使食物中的Fe3+转化为Fe2+,Fe元素的化合价降低,则维生素C中某元素的化合价升高;
(2)由总反应可知,亚铁离子不是反应物,也不是生成物.
解答 解:(1)维生素C可使食物中的Fe3+转化为Fe2+,Fe元素的化合价降低,则维生素C中某元素的化合价升高,则维生素C为还原剂,具有还原性,
故答案为:还原;还原;
(2)由总反应可知,亚铁离子不是反应物,也不是生成物,则在整个反应中,Fe2+实际上起着催化剂的作用,故答案为:催化剂.
点评 本题考查氧化还原反应,涉及亚铁和铁离子的转化、维生素C的作用等,明确反应中元素的化合价变化结合氧化还原反应即可解答,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
7.下列离子方程式正确的是( )
| A. | 碳酸钙和盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| B. | 向氢氧化钡溶液中加入硫酸溶液 SO42-+Ba2+═BaSO4↓ | |
| C. | 向稀盐酸溶液中加铁 3Fe+6H+═3H2↑+3Fe3+ | |
| D. | 向硝酸银溶液中加盐酸 Ag++Cl-═AgCl↓ |
8. 将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.
将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.
 将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.
将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.| x值 | y=f(x) |
| 0<x≤3 | y=$\frac{2}{3}$x |
| 3<x<3.2 | y=32-10x |
| - | - |
| - | - |
5.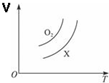 如图表示1g O2与1g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
如图表示1g O2与1g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
 如图表示1g O2与1g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
如图表示1g O2与1g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )| A. | C2H4 (气) | B. | CH4 | C. | CO2 | D. | NO |
9.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是( )
| A. | NH4+、Cu2+、Cl-、NO3- | B. | Ba2+、Mg2+、HCO3-、Br- | ||
| C. | K+、Na+、CO32-、SO42- | D. | K+、Na+、SO32-、S2- |
6.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 饱和氯水中:NH4+、SO32-、SO42-、Cl- | |
| C. | c(H+)=1.0×10-13mol/L溶液中:K+、Na+、CH3COO-、Br- | |
| D. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |