题目内容
5.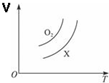 如图表示1g O2与1g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
如图表示1g O2与1g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )| A. | C2H4 (气) | B. | CH4 | C. | CO2 | D. | NO |
分析 压强相同、温度相同时,气体体积与物质的量成正比,根据图象知,相同温度下,氧气体积大于X气体,说明氧气的物质的量大,根据n=$\frac{m}{M}$判断X摩尔质量相对大小,据此分析解答.
解答 解:压强相同、温度相同时,气体体积与物质的量成正比,根据图象知,相同温度下,氧气体积大于X气体,说明氧气的物质的量大,根据n=$\frac{m}{M}$知,质量相同时,物质的量与摩尔质量成反比,氧气的物质的量大于X,则氧气的摩尔质量小于X,这几个选项中只有二氧化碳摩尔质量大于氧气,
故选C.
点评 本题考查阿伏伽德罗定律及其推论,明确P、V、n、T、M之间的关系是解本题关键,会分析图象中曲线变化趋势,采用“定一议二”的方法分析,题目难度中等.

练习册系列答案
相关题目
15.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LNO与0.5molO2充分反应,最后得到NA个NO2分子 | |
| B. | 1.0L 0.5mol/L的NaAlO2水溶液中含有氧原子数为NA | |
| C. | 常温常压下,14g的C2H4和C4H8混合气体中含有的原子数为3NA | |
| D. | 某密闭容器盛有0.2molSO2和0.1molO2,在一定条件下充分反应,转移电子的数目为0.4NA |
13.实验中需1mol•L-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是( )
| A. | 1000 mL,106.0g | B. | 950 mL,100.7g | C. | 950 mL,106.0g | D. | 1000 mL,100.7 g |
20.设NA为阿伏加德罗常数的值,N表示粒子数.下列说法正确的是( )
| A. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| B. | 将1mol Cl2溶解于水中,则溶液中有N(HClO)+N(Cl-)+N(ClO-)=2[NA-N(Cl2)] | |
| C. | 一定条件下,0.1mol H2与足量氮气反应生成NH3,转移电子数为0.2NA | |
| D. | 电解精炼铜,当阳极质量减少3.2g时,电路中通过的电子数目为0.1NA |
10.环境污染已成为人类社会面临的重大威胁.下列有关环境问题的说法正确的是( )
| A. | pH在5.6~7.0之间的降水通常称作酸雨 | |
| B. | 臭氧的体积分数超过10-4%的空气有利于人体健康 | |
| C. | 燃烧煤时加入适量石灰石,可减少废气中二氧化硫含量 | |
| D. | 含磷的合成洗涤剂易于被细菌分解,故不会导致水体污染 |
15.若NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1 molCl2参加反应转移电子数一定为2 NA | |
| B. | 将31g的Na2O溶解于1L水中,所得溶液中Na+的物质的量浓度为1 mol/L | |
| C. | 22.4L的NH3 和16g CH4中所含有的电子数都是10NA | |
| D. | 20g重水(2H216O)含有的电子数为10NA |
