题目内容
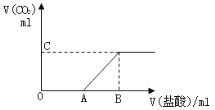
【题目】标准状况下,向100 mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得最后所得溶液M的PH>7(反应前后溶液的体积变化忽略不计)。在溶液M中逐滴缓慢滴加1 mol/L盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
已知图中B点位置固定,且V(B)=300,而点A C 可在各自的轴上移动。
(1)原溶液的物质的量浓度为_________mol/L,B点时,最终所得溶液中的溶质的物质的量浓度是___________mol/L(两种溶液混合时体积可以直接相加)
(2)V(A)的取值不同时,溶液M中的溶质的成分也不同,请填写下表:
V(A)的取值 | V(A)=0 | 0<V(A)<150 | V(A)=150 | 150<V(A)<300 |
溶质的成分 | ①__________ | ②___________ | ③_________ | ④_____________ |
当V(A)=200时,C点数值为_____________。
(3)取V(A)=100时对应的溶液M 30ml 与等体积的1 mol/L的盐酸按各种可能的方式混合,产生的气体体积Vml,则V 的取值范围是___________________。
【答案】3 0.75 NaHCO3 Na2CO3和NaHCO3 Na2CO3 NaOH和Na2CO3 2240 0≤V≤448
【解析】
向100 mLNaOH溶液中缓慢通入一定量的CO2气体,发生反应:
2NaOH+CO2=Na2CO3+H2O,Na2CO3+CO2+H2O==2NaHCO3
在生成的M溶液中滴加盐酸,发生如下反应:
OA段,NaOH+HCl=NaCl+H2O,Na2CO3+HCl=NaCl+ NaHCO3
AB段,NaHCO3+HCl=NaCl+H2O+CO2↑,据此分析作答
(1)从B点切入,因为此时产物为NaCl,所以n(NaCl)=n(NaOH)=1mol/L×0.3L=0.3mol。
原溶液的物质的量浓度为![]() mol/L。答案为:3;
mol/L。答案为:3;
B点时,最终所得溶液中的溶质的物质的量浓度是![]() mol/L。
mol/L。
答案为:0.75;
(2)V(A)的取值不同时,溶液M中的溶质的成分也不同,请填写下表:
V(A)的取值 | V(A)=0 | 0<V(A)<150 | V(A)=150 | 150<V(A)<300 |
溶质的成分 | ①__________ | ②___________ | ③_________ | ④_____________ |
从表中可以看出,V(A)=0时,①溶质为NaHCO3。答案为:①NaHCO3
当0<V(A)<150时,②溶质为Na2CO3和NaHCO3。答案为:②Na2CO3和NaHCO3
当V(A)=150时,③溶质为Na2CO3。答案为:③Na2CO3
当150<V(A)<300,④溶质为NaOH和Na2CO3。答案为:④NaOH和Na2CO3
当V(A)=200时,C点溶质为NaOH和Na2CO3,且二者的物质的量之比为1:1。
则AB段发生的反应为:NaHCO3+HCl=NaCl+H2O+CO2↑
0.1L×1mol/L 0.1mol
V(CO2)=0.1mol×22.4L/mol=2.24L=2240mL
答案为:2240;
(3)由上面分析知,V(A)=100时对应的溶液M中,溶质为Na2CO3和NaHCO3,二者的物质的量之比为1:1,且二者的浓度都是1mol/L。
若将盐酸加入M溶液中,n(Na2CO3)= 1mol/L×0.03L=0.03mol,
n(NaHCO3)= 1mol/L×0.03L=0.03mol,n(HCl)= 1mol/L×0.03L=0.03mol。
发生反应为Na2CO3+HCl=NaCl+ NaHCO3
0.03mol 0.03mol
盐酸将Na2CO3转化为NaHCO3便消耗完,所以生成二氧化碳的体积为0。
若将M溶液滴入盐酸中,发生反应为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑
0.01mol 0.02mol 0.01mol 0.01mol 0.01mol 0.01mol
共生成CO2气体的体积为:0.02mol×22400mL/mol=448mL
故取V(A)=100时对应的溶液M 30mL与等体积的1 mol/L的盐酸按各种可能的方式混合,产生的气体体积VmL,则V 的取值范围是0≤V≤448
答案为:0≤V≤448;

 教材全解字词句篇系列答案
教材全解字词句篇系列答案

