��Ŀ����
(13��)��������͵��������dz��õĻ���ԭ�ϣ�Ҳ�����������������Ⱦ���ۺ���������Ⱦ�ǻ�����ѧ��ǰ����Ҫ�о�����֮һ��
��1������β������Ҫ����CO��NO2��SO2��CO2���壬���� �ܵ��¹⻯ѧ�������γɣ�
Ŀǰ���õ�������������װ���а�װһ����������������Ч�Ľ�β���е��к�����ת�����磺CO��g��+NO2��g�� NO��g��+CO2��g�� ��H=��akJ��mol��1��a>0��2CO��g��+2NO2��g�� N2��g��+2CO2��g�� ��H=��bkJ��mol��1��b>0��
�ݴ˻ش����ñ�״����3.36��CO��ԭNO2��N2��CO��ȫ��Ӧ��������������ת�Ƶ��ӵ����ʵ���Ϊ mol���ų�������Ϊ kJ���ú���a��b�Ĵ���ʽ��ʾ����
�����Ͱ��������������Ļ�ѧԭ���Dz��ð�ˮ���������е�SO2������һ�������������������ղ��ﷴӦ���ü������ŵ�����ܻ�������SO2�⣬���ܵõ�һ�ָ��Ϸ��ϣ��ø��Ϸ��Ͽ��ܵĻ�ѧʽΪ ��ֻҪ��дһ�֣���
��3����ҵ����������ʱ����SO2����ΪSO3�ǹؼ�һ����
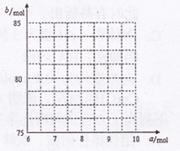
��ij�¶��£�SO2��g����1/2O2��g��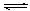 SO3��g������H=" ��98" kJ�� mol��1����ʼʱ��10L���ܱ������м���4.0mol SO2(g)��5.0molO2(g)������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K= ��
SO3��g������H=" ��98" kJ�� mol��1����ʼʱ��10L���ܱ������м���4.0mol SO2(g)��5.0molO2(g)������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K= ��
��һ�������£���һ���������ܱ������г���2molSO2��1molO2���������з�Ӧ��2SO2��g����O2��g��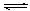 2SO3��g���ﵽƽ���ı���������SO3�����������������
2SO3��g���ﵽƽ���ı���������SO3�����������������
A�������¶Ⱥ�����ѹǿ���䣬����2mol SO3����
B�������¶Ⱥ�����������䣬����2mol N2
C�������¶Ⱥ�����������䣬����0.5mol SO2��0.25mol O2
E�������¶� F���ƶ�����ѹ������
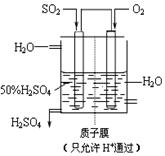
��4��ij������������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��SO2�ĵ缫�ĵ缫��Ӧʽ��
��
��1������β������Ҫ����CO��NO2��SO2��CO2���壬���� �ܵ��¹⻯ѧ�������γɣ�
Ŀǰ���õ�������������װ���а�װһ����������������Ч�Ľ�β���е��к�����ת�����磺CO��g��+NO2��g��
�ݴ˻ش����ñ�״����3.36��CO��ԭNO2��N2��CO��ȫ��Ӧ��������������ת�Ƶ��ӵ����ʵ���Ϊ mol���ų�������Ϊ kJ���ú���a��b�Ĵ���ʽ��ʾ����
�����Ͱ��������������Ļ�ѧԭ���Dz��ð�ˮ���������е�SO2������һ�������������������ղ��ﷴӦ���ü������ŵ�����ܻ�������SO2�⣬���ܵõ�һ�ָ��Ϸ��ϣ��ø��Ϸ��Ͽ��ܵĻ�ѧʽΪ ��ֻҪ��дһ�֣���
��3����ҵ����������ʱ����SO2����ΪSO3�ǹؼ�һ����
��ij�¶��£�SO2��g����1/2O2��g��
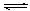 SO3��g������H=" ��98" kJ�� mol��1����ʼʱ��10L���ܱ������м���4.0mol SO2(g)��5.0molO2(g)������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K= ��
SO3��g������H=" ��98" kJ�� mol��1����ʼʱ��10L���ܱ������м���4.0mol SO2(g)��5.0molO2(g)������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K= ����һ�������£���һ���������ܱ������г���2molSO2��1molO2���������з�Ӧ��2SO2��g����O2��g��
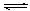 2SO3��g���ﵽƽ���ı���������SO3�����������������
2SO3��g���ﵽƽ���ı���������SO3����������������� A�������¶Ⱥ�����ѹǿ���䣬����2mol SO3����
B�������¶Ⱥ�����������䣬����2mol N2
C�������¶Ⱥ�����������䣬����0.5mol SO2��0.25mol O2
E�������¶� F���ƶ�����ѹ������
��4��ij������������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��SO2�ĵ缫�ĵ缫��Ӧʽ��
��

��1��NO2��0.3�� 3(2a+b)/80
��(NH4)3PO4����(NH4)2HPO4��NH4H2PO4��
��3����2.5 mol��1��L
��CF
��4��SO2+ 2H2O�� SO42��+4 H+ + 2e��
��(NH4)3PO4����(NH4)2HPO4��NH4H2PO4��
��3����2.5 mol��1��L
��CF
��4��SO2+ 2H2O�� SO42��+4 H+ + 2e��
��

��ϰ��ϵ�д�
 ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
�����Ŀ
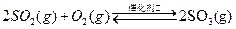

 ��
�� �����
����� ,
,
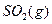 ������
������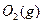 ��ַ�Ӧ����
��ַ�Ӧ����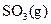 ���ų�����
���ų����� 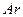 b����ƽ�������г���
b����ƽ�������г���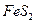 ��ȫ����
��ȫ����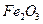 ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����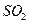 ��
��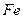 ��
�� �����ʵ���֮��n(
�����ʵ���֮��n( ��
�� mol��
mol�� CO����H2O�У�ŨH2SO4ֻ������ˮ��
CO����H2O�У�ŨH2SO4ֻ������ˮ�� CuSO4+SO2��+2H2O�У�ŨH2SO4ֻ����������
CuSO4+SO2��+2H2O�У�ŨH2SO4ֻ����������