题目内容
下列叙述正确的是
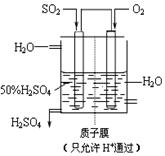
①标准状况下,1molSO2和1molSO3的体积相同;②SO2通入BaCl2溶液中不会有沉淀生成;③SO2有漂白性,而湿润的氯气也有漂白性,因此将SO2和Cl2以等物质的量混合后漂白作用更强;④SO2既有氧化性又有还原性;⑤SO2通入Ba(OH)2溶液中有白色沉淀生成,若加入足量的稀硝酸,沉淀将全部溶解
①标准状况下,1molSO2和1molSO3的体积相同;②SO2通入BaCl2溶液中不会有沉淀生成;③SO2有漂白性,而湿润的氯气也有漂白性,因此将SO2和Cl2以等物质的量混合后漂白作用更强;④SO2既有氧化性又有还原性;⑤SO2通入Ba(OH)2溶液中有白色沉淀生成,若加入足量的稀硝酸,沉淀将全部溶解
| A.①② | B.②④⑤ | C.②④ | D.③⑤ |
C
略

练习册系列答案
相关题目
 白色沉淀
白色沉淀 白色沉淀。
白色沉淀。 白色沉淀。
白色沉淀。 无色溶液
无色溶液
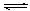 SO3(g);△H=" —98" kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K= 。
SO3(g);△H=" —98" kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K= 。