题目内容
【题目】改变a1mol/L元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示,已知[δ(X)= ![]() ]。
]。
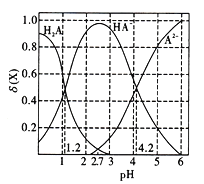
下列叙述错误的是
A. lg[K2(H2A)]=-4.2;pH=2.7时,c(HA-)>c(H2A)=c(A2-)
B. pH=4.2时,c(HA-)=c(A2-)>c(H+);随着pH的升高,c(HA-)/c(H2A)的比值先增大后减小
C. 0.1mol/L的NaHA溶液中存在:c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2mol/L
D. pH=1.2时,c(H2A)=c(HA-)
【答案】B
【解析】根据图示所知,在溶液的pH=4.2时,c(H+)=10-4.2mol/L,c(A2-)= c(HA-) ,根据[K2(H2A)]=c(A2-)×c(H+)/ c(HA-)=10-4.2,lg[K2(H2A)]=-4.2;当pH=2.7时,据图像可知:c(HA-)>c(H2A)=c(A2-),A正确;pH=4.2时,c(HA-)=c(A2-)>c(H+),随着pH的升高,酸性减弱,H2A电离程度增大,c(HA-)/c(H2A)的比值增大,B错误;0.1mol/L的NaHA溶液中,根据物料守恒可知c(A2-)+c(H2A)+c(HA-)=0.1 mol/L,c(Na+)=0.1 mol/L,所以c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2mol/L,C正确;从图像可知:pH=1.2时,c(H2A)、c(HA-)的δ(X)相等,所以c(H2A)=c(HA-),D正确;正确选项B。

 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案【题目】将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数 | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | 8 |
下列说法不正确的是
A. x=1.6
B. 实验1在前6min 的反应速率v (SO2)=0.2mol·L-1·min-1
C. T1、T2的关系:T1>T2
D. K1、K2的关系:K1 >K2