题目内容
【题目】一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)![]() CH3OH(g) △H=akJ·mol-1,△S=bJ·mol-1·K-1 (a、b均为正数),达到化学平衡状态。
CH3OH(g) △H=akJ·mol-1,△S=bJ·mol-1·K-1 (a、b均为正数),达到化学平衡状态。

(1)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是_______(用nB、tB表示)。
(2)判断该可逆反应达到化学平衡状态的标志是_____________(填字母)。
a.2v生成(CH3OH)=v生成(H2) b.压强不变
c.混合气体的密度不再改变 d.CO的体积分数不再变化
(3)如果反应从逆反应开始,将CH3OH充入容器a和b中进行反应。a的容积保持不变,b的上盖可随容器内气体压强的改变而上下移动,以保持容器内外压强相等。同温同压时,将等量的CH3OH充入初始体积相同的容器a、b中,反应同时开始。反应开始时,a与b中生成H2的速率va_______vb,反应过程中两容器里生成H2的速率是va_______vb,达到平衡时,a与b中CH3OH转化率相比较,则是aa______ab
【答案】 ![]() mol·L-1·min-1 abd = > <
mol·L-1·min-1 abd = > <
【解析】(1)υ(CH3OH)= ![]() mol/(L·min),故υ(H2)=2υ(CH3OH)=
mol/(L·min),故υ(H2)=2υ(CH3OH)= ![]() mol/(L·min),故答案为:
mol/(L·min),故答案为: ![]() mol/(L·min);
mol/(L·min);
(2)2v生成(CH3OH)=v生成(H2),体现此时甲醇的正逆反应速率相等,达到平衡;两边的化学计量数和不等,压强不变是平衡状态;混合气体质量和体积始终不改变,气体的密度不变,不能作为判断是否达到平衡状态的依据;CO的浓度体积分数不再改变,说明达到平衡状态;故答案为:abd;
(3)反应起始时,两容器中甲醇的浓度相等,所以两容器中生成H2的速率关系是va=vb;因为该反应是体积增大的反应,b是恒压,而a是恒容,所以在反应过程中a的压强大于b,压强大反应速率也大,所以生成H2的速率关系是va>vb;因为该反应是体积增大的反应,b是恒压,而a是恒容,所以再达到平衡时,a的压强大于b,B容器中反应正向进行的程度大于A,所以甲醇的转化率大小关系是:αa<αb,故答案为:=;>;<。

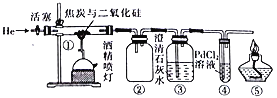
【题目】利用下图所示装置进行下列实验,其中丙中实验现象描述正确的是

实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
A | 浓硫酸 | 亚硫酸钠 | 紫色石蕊试液 | 溶液先变红后褪色 |
B | 浓盐酸 | 高锰酸钾 | 淀粉碘化钾溶液 | 溶液会变蓝 |
C | 稀盐酸 | 碳酸钙 | 氯化钡溶液 | 有白色沉淀生成 |
D | 浓氨水 | 氧化钙 | 氯化铝溶液 | 先生成白色沉淀然后沉淀溶解 |
A. A B. B C. C D. D