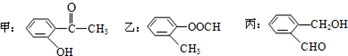
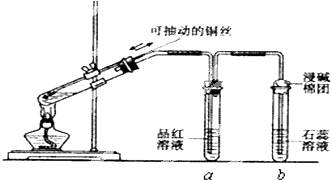
题目内容
12.陈先生有一套珍贵的铜制餐具,使用一段时间后餐具会变黑,陈先生会把餐具加热后用无水酒精浸泡,之后餐具便会光洁如新.请写出以上过程的所有化学方程式2Cu+O2=2CuO、CuO+CH3CH2OH→Cu+CH3CHO+H2O.分析 餐具会变黑生成CuO,CuO可氧化酒精,本身被还原,以此来解答.
解答 解:铜制餐具,使用一段时间后餐具会变黑,发生2Cu+O2=2CuO,餐具加热后用无水酒精浸泡,之后餐具便会光洁如新,发生CuO与乙醇的氧化还原反应,反应为CuO+CH3CH2OH→Cu+CH3CHO+H2O,
故答案为:2Cu+O2=2CuO、CuO+CH3CH2OH→Cu+CH3CHO+H2O.
点评 本题考查铜及其化合物的性质,为高频考点,把握Cu、CuO的性质及发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
17.H2和I2在一定条件下能发生反应:H2(g)+I2(g)═2HI(g)△H=-a kJ•mol-1已知: (a、b、c均大于零)下列说法不正确的是( )
(a、b、c均大于零)下列说法不正确的是( )
 (a、b、c均大于零)下列说法不正确的是( )
(a、b、c均大于零)下列说法不正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a) kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
4.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式: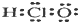 | B. | 氯化钠的分子式:NaCl | ||
| C. | 二氧化碳的比例模型: | D. | Cl-的结构示意图: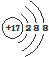 |
2.电解法炼铝时,冰晶石的作用是( )
| A. | 助熔剂 | B. | 催化剂 | C. | 还原剂 | D. | 氧化剂 |