题目内容
【题目】按要求回答下列问题:
(1)硫酸工业生产中,反应产生SO2气体的设备名称___。
(2)以下物质中:①H2SO4,②CaCl2,③NaHS,④He,⑤镁。
化学键只含共价键的是___;只含离子键的是___。
(3)用双桥表示3Cl2+6KOH=5KCl+KClO3+3H2O电子转移的方和数目:___。
(4)在一定条件下,利用置换反应X+Y=W+Z,可实现物质之间的转化
①若X为Mg,W为C,则Z为(填化学式)___。
②若X为SiO2,工业上利用焦炭还原二氧化硅的化学方程式___。
【答案】沸腾炉 ① ② 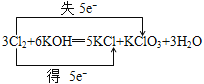 MgO SiO2+2C
MgO SiO2+2C![]() Si+2CO↑
Si+2CO↑
【解析】
(1)根据黄铁矿的主要成分为FeS2,煅烧时与O2反应生成Fe2O3和SO2,结合硫酸工业使用的设备回答;
(2)活泼金属和活泼非金属之间易形成离子键,非金属之间易形成共价键,据此分析解答;
(3)根据化合价的变化结合氧化还原反应的规律分析解答;
(4)①Mg与二氧化碳发生置换反应生成C和MgO;②焦炭高温下可以还原二氧化硅生成一氧化碳和硅,据此分析解答。
(1)黄铁矿的主要成分为FeS2,煅烧时与O2反应生成Fe2O3和SO2,黄铁矿煅烧的设备是沸腾炉,故答案为:沸腾炉;
(2)①H2SO4为共价化合物,只存在共价键;
②CaCl2是离子化合物,只含离子键;
③NaHS是离子化合物,含有离子键和共价键;
④氦气为单原子分子,无任何化学键;
⑤镁是金属单质,含有金属键;
只含共价键的是①;只含离子键的物质是②,故答案为:①;②;
(3)3Cl2+6KOH═5KCl+KClO3+3H2O中失电子的Cl元素化合价升高,得电子的Cl元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目=5,电子转移情况为: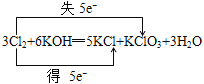 ,故答案为:
,故答案为: ;
;
(4)①若X为Mg,W为C,则Mg与二氧化碳发生置换反应生成C和MgO,所以Z为MgO,故答案为:MgO;
②若X为SiO2,焦炭高温还原二氧化硅生成一氧化碳和硅,化学方程式:SiO2+2C ![]() Si+2CO↑,故答案为:SiO2+2C
Si+2CO↑,故答案为:SiO2+2C ![]() Si+2CO↑。
Si+2CO↑。

 口算能手系列答案
口算能手系列答案