题目内容
14.某芳香族化合物A的分子式为C8H8O3,其苯环上的一卤代物有两种同分异构体.如图表示化合物A~H之间的转化关系,其中化合物G能发生银镜反应.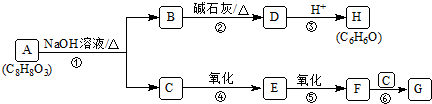
请回答:
(1)A的结构简式
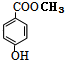 .
.(2)反应⑥的化学方程式
 .
.(3)反应①的离子方程式
 +2OH-$\stackrel{△}{→}$
+2OH-$\stackrel{△}{→}$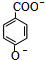 +CH3OH+H2O.
+CH3OH+H2O.(4)检验化合物H的试剂是浓溴水(或FeCl3溶液),化合物H和E反应的化学方程式
 ,该反应类型是缩聚.
,该反应类型是缩聚.(5)写三种A的同分异构体的结构简式(要求所写结构式苯环上取代基数目各不相同)
 .
.
分析 C能经过两步氧化得F,F与C反应生成G,G能发生银镜反应,则说明C为CH3OH,E为HCHO,F为HCOOH,G为HCOOCH3,某芳香族化合物A的分子式为C8H8O3,A能与氢氧化钠溶液反应生成B和C,其苯环上的一卤代物有两种同分异构体,说明有A中有酯基,且有两个处于对位的基团,根据H的分子式可知,H为苯酚,结合各物质转化关系,结合A的分子式和C的结构可知,A为 ,B为
,B为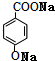 ,B与碱石灰加热得D为
,B与碱石灰加热得D为 ,D酸化得H为
,D酸化得H为 ,据此答题.
,据此答题.
解答 解:C能经过两步氧化得F,F与C反应生成G,G能发生银镜反应,则说明C为CH3OH,E为HCHO,F为HCOOH,G为HCOOCH3,某芳香族化合物A的分子式为C8H8O3,A能与氢氧化钠溶液反应生成B和C,其苯环上的一卤代物有两种同分异构体,说明有A中有酯基,且有两个处于对位的基团,根据H的分子式可知,H为苯酚,结合各物质转化关系,结合A的分子式和C的结构可知,A为 ,B为
,B为 ,B与碱石灰加热得D为
,B与碱石灰加热得D为 ,D酸化得H为
,D酸化得H为 ,
,
(1)根据上面的分析可知,A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)反应⑥的化学方程式为  ,
,
故答案为: ;
;
(3)反应①的离子方程式为 +2OH-$\stackrel{△}{→}$
+2OH-$\stackrel{△}{→}$ +CH3OH+H2O,故答案为:
+CH3OH+H2O,故答案为: +2OH-$\stackrel{△}{→}$
+2OH-$\stackrel{△}{→}$ +CH3OH+H2O;
+CH3OH+H2O;
(4)检验 的试剂是 浓溴水(或FeCl3溶液),
的试剂是 浓溴水(或FeCl3溶液), 和HCHO反应生成酚苯树脂,反应的化学方程式 为
和HCHO反应生成酚苯树脂,反应的化学方程式 为 ,该反应类型是缩聚,
,该反应类型是缩聚,
故答案为:浓溴水(或FeCl3溶液); ;
;
(5)A为 ,A的同分异构体的结构简式(要求所写结构式苯环上取代基数目各不相同)为
,A的同分异构体的结构简式(要求所写结构式苯环上取代基数目各不相同)为
故答案为:
点评 本题考查有机物的推断,掌握官能团的性质是关键,C可以连续氧化生成的F与反应生成G能发生银镜反应为突破口,再根据H和A的分子式进行推断,综合考查学生的能力,难度中等.

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案| A. | 0.1 | B. | 0.15 | C. | 0.2 | D. | 0.25 |
| A. | 甲酸 | B. | 葡萄糖 | C. | 蔗糖 | D. | 甲酸异丙酯 |
| A. | 已知2SO2(g)+O2?2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)=2CO2 (g)△H1 2C(s)+O2(g)=2CO(g)△H2则△H1<△H2 | |
| D. | 已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和的反应热均为57.3kJ |
| A. | NaClO溶液中通入少量SO2:ClO-+SO2+H2O=2H++SO42-+Cl- | |
| B. | FeCl3溶液中通入过量H2S气体:2Fe3++3H2S=2FeS↓+S↓+6H+ | |
| C. | Na2CO3溶液中通入少量Cl2:2CO32-+Cl2+H2O=ClO-+Cl-+2HCO3- | |
| D. | NaHSO3溶液中通入少量Cl2:HSO3-+Cl2+H2O=3H++SO42-+2Cl- |
 甲、乙、丙、丁的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是
甲、乙、丙、丁的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | Fe | FeCl3 | Fe(OH)3 | Fe2O3 |
| B | Al | Al(OH)3 | Al2O3 | NaAlO2 |
| C | NaCl | Na | Na2O2 | Na2CO3 |
| D | SiO2 | H2SiO3 | Na2SiO3 | Si |
| A. | A | B. | B | C. | C | D. | D |
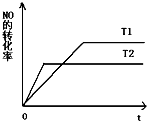 近年来北京市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.
近年来北京市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.