��Ŀ����
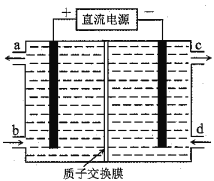
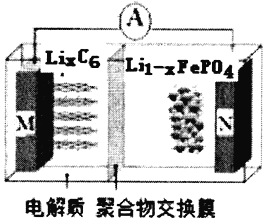
����Ŀ�����ǵϴ��綯��������һ�־��и�Ч��������ɿ��ٳ�硢�Ի�������Ⱦ���ŵ����͵�أ��乤��ԭ����ͼ��M�缫�����ǽ���﮺�̼�ĸ��ϲ���(̼��Ϊ����﮵�����)�������Ϊһ���ܴ���Li+�ĸ߷��Ӳ��ϣ��ۺ��サ��Ĥֻ����Li+ͨ������e-����ͨ������ط�ӦʽΪLixC6+Li1-xFePO4![]() LiFePO4+6C������˵������ȷ����
LiFePO4+6C������˵������ȷ����
A. �ŵ�ʱ��N�����������缫��ӦʽΪLi(1-x)FePO4+xLi++xe-=LiFePO4
B. ���ʱ��Li+ͨ���ۺ��サ��Ĥ��M��Ǩ��
C. �øõ�ص�⾫��ͭ��������������19.2gʱ��ͨ���ۺ��サ��Ĥ��Li+��ĿΪ0.6NA
D. ���ʱ��·��ͨ��0.5mol e-������36gC
���𰸡�D
����������Ӧ����ʽΪ��LixC6+Li1-xFePO4![]() LiFePO4+6C������LixC6ת��ΪC��˵���������Liʧȥ����ת��ΪLi+������Ǩ������������淢��ʧ���ӵ�������Ӧ����LixC6Ϊ������M��������Li1-xFePO4Ϊ������N������Ӧ��Li1-xFePO4ת��ΪLiFePO4�����Է�ӦΪ��Li(1-x)FePO4+xLi++xe-=LiFePO4��ѡ��A��ȷ������ǵ��أ�������Ӧ�����������������ƶ�������ѡ��B��ȷ����⾫��ͭ��ʱ���������ӵ�������Cu���������ӵ�ͭΪ19.2g��0.3mol����ת�Ƶ���Ϊ0.6mol����Ϊ����Ӵ�һ����λ������ɣ�ͨ������Ĥ�������һ��Ϊ0.6mol��ѡ��C��ȷ���õ�صķ�Ӧ��﮵��ʺ������֮���ת����Cֻ����Ϊ����﮵����壬��Ӧǰ��û�б仯��ѡ��D����
LiFePO4+6C������LixC6ת��ΪC��˵���������Liʧȥ����ת��ΪLi+������Ǩ������������淢��ʧ���ӵ�������Ӧ����LixC6Ϊ������M��������Li1-xFePO4Ϊ������N������Ӧ��Li1-xFePO4ת��ΪLiFePO4�����Է�ӦΪ��Li(1-x)FePO4+xLi++xe-=LiFePO4��ѡ��A��ȷ������ǵ��أ�������Ӧ�����������������ƶ�������ѡ��B��ȷ����⾫��ͭ��ʱ���������ӵ�������Cu���������ӵ�ͭΪ19.2g��0.3mol����ת�Ƶ���Ϊ0.6mol����Ϊ����Ӵ�һ����λ������ɣ�ͨ������Ĥ�������һ��Ϊ0.6mol��ѡ��C��ȷ���õ�صķ�Ӧ��﮵��ʺ������֮���ת����Cֻ����Ϊ����﮵����壬��Ӧǰ��û�б仯��ѡ��D����