题目内容
【题目】某研究小组利用氮气、氧化铝和活性炭制取氮化铝,设计如图1所示实验装置。
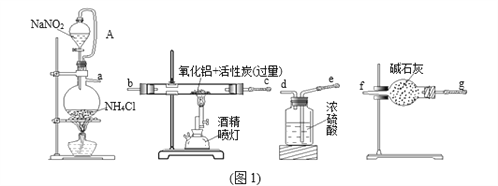
请回答:
(1)图1装置中各仪器导管口连接的顺序是(可重复使用,用小写字母a→g填写):___________;导管A的作用是_________________________。
(2)图1中用饱和NaNO2溶液与NH4Cl溶液加热制取氮气,该离子方程式为________。
(3)硬质试管中生成AlN的反应方程式是_________________________。
(4)按要求连接的实验装置,存在严重问题,请说明改进的办法,存在的缺陷是______,改进的办法是_____________________________________________。
(5)反应结束后,某同学用图2装置进行实验来测定氮化铝样品的质量分数(实验中导管体积忽略不计)。
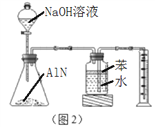
①氮化铝与过量的NaOH溶液反应生成氨气化学反应方程式为___________________;
②集气瓶中的苯的作用是______________________;集气瓶中的液体没有装满,实验测得NH3的体积将__________(填“偏大”“偏小”或“不变”)。
③若实验中称取氮化铝样品的质量为8.0 g,测得氨气的体积2.8 L(标准状况),则样品中AlN的质量分数为___________(保留3位有效数字)。
【答案】 NO2—+ NH4+ ![]() 2H2O + N2↑ a-e-d-g-f-c-b(或b-c) -g-f 平衡分液漏斗与烧瓶之间的压强,使NaNO2 饱和溶液顺利滴下 N2 + Al2O3 + 3C
2H2O + N2↑ a-e-d-g-f-c-b(或b-c) -g-f 平衡分液漏斗与烧瓶之间的压强,使NaNO2 饱和溶液顺利滴下 N2 + Al2O3 + 3C ![]() 2AlN + 3CO 没有尾气处理装置,会污染大气 在干燥管末端连一尾气处理装置 AlN+NaOH+H2O===NaAlO2+NH3↑ 防止氨气溶于水 不变 64.1%
2AlN + 3CO 没有尾气处理装置,会污染大气 在干燥管末端连一尾气处理装置 AlN+NaOH+H2O===NaAlO2+NH3↑ 防止氨气溶于水 不变 64.1%
【解析】试题分析:本题以利用氮气、氧化铝和活性炭制取氮化铝为载体,考查N2的制备,实验装置的连接,物质的含量测定,实验方案的设计和评价。根据原子守恒,由饱和NaNO2溶液与NH4Cl溶液加热制取氮气的同时还有NaCl和H2O生成,,制备N2的反应原理为NaNO2+NH4Cl![]() N2↑+NaCl+2H2O;由于NH4Cl受热会分解成NH3和HCl,使得所得N2中混有H2O(g)、NH3、HCl,所以N2与氧化铝和活性炭反应之前必须除去这些杂质气体,除杂时先通过浓硫酸吸收NH3和H2O(g),再通过碱石灰吸收HCl;接着干燥纯净的N2与氧化铝和活性炭反应制得AlN;但由于AlN易水解,所以最后还要用盛放碱石灰的干燥管吸收空气中的水蒸气,防止水蒸气进入硬质试管中使AlN发生水解,则图1装置中各仪器导管口连接的顺序为a-e-d-g-f-c-b(或b-c) -g-f。
N2↑+NaCl+2H2O;由于NH4Cl受热会分解成NH3和HCl,使得所得N2中混有H2O(g)、NH3、HCl,所以N2与氧化铝和活性炭反应之前必须除去这些杂质气体,除杂时先通过浓硫酸吸收NH3和H2O(g),再通过碱石灰吸收HCl;接着干燥纯净的N2与氧化铝和活性炭反应制得AlN;但由于AlN易水解,所以最后还要用盛放碱石灰的干燥管吸收空气中的水蒸气,防止水蒸气进入硬质试管中使AlN发生水解,则图1装置中各仪器导管口连接的顺序为a-e-d-g-f-c-b(或b-c) -g-f。
(1)图1装置中各仪器导管口连接的顺序为a-e-d-g-f-c-b(或b-c) -g-f。由于蒸馏烧瓶中有气体产生,压强增大,分液漏斗中的液体不易滴下;使用导管A将蒸馏烧瓶和分液漏斗相连,压强相同,便于液体顺利滴下。导管A的作用是:平衡分液漏斗与烧瓶之间的压强,使NaNO2 饱和溶液顺利滴下。
(2)制备N2的离子方程式为NO2-+NH4+![]() N2↑+2H2O。
N2↑+2H2O。
(3)由于活性炭是过量的,结合原子守恒,N2与氧化铝和活性炭反应时除生成AlN外还生成CO,反应的化学方程式为N2+Al2O3+3C![]() 2AlN+3CO。
2AlN+3CO。
(4)由反应原理知,制得AlN的同时生成了CO;若按要求连接的实验装置,存在的严重问题是没有尾气处理装置,CO污染大气。改进的方法是在干燥管末端连一尾气处理装置。
(5)①根据原子守恒以及NaOH过量,AlN与过量NaOH溶液反应生成NH3和NaAlO2,反应的化学方程式为AlN+NaOH+H2O=NaAlO2+NH3↑。
②用排水法测量生成NH3的体积,由于NH3极易溶于水,能被水吸收,无法测量NH3的体积,用苯将NH3和水隔开防止氨气溶于水,所以苯的作用是防止氨气溶于水。由于排出水的体积等于收集到氨气的体积是按压强原理完成的,所以若集气瓶中的液体没有装满,实验测得NH3的体积不变。
③根据N守恒,n(AlN)=n(NH3)=![]() =0.125mol,m(AlN)=0.125mol
=0.125mol,m(AlN)=0.125mol![]() 41g/mol=5.125g,样品中AlN的质量分数为
41g/mol=5.125g,样品中AlN的质量分数为![]() 100%=64.1%。
100%=64.1%。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】一定温度下,在4个容积均为1 L的恒容容器中分别进行反应(各容器中A都足量)A(s)+B(g)![]() C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
容器编号 | n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min | 反应速率 |
Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
Ⅱ | 0.12 | 1.20 | 0.20 | t2 | |
Ⅲ | 0.32 | 1.0 | 0 | 0 | |
Ⅳ | 0.12 | 0.30 | v(正)=v(逆) |
下列说法正确的是
A.容器Ⅰ中平均反应速率v(B)=0.04/t1 mol·L-1·min-1
B.t2时容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ
D.容器Ⅳ中c(D)= 0.4 mol·L-1