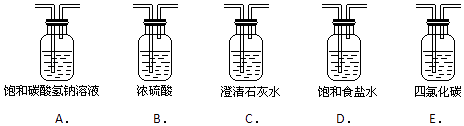
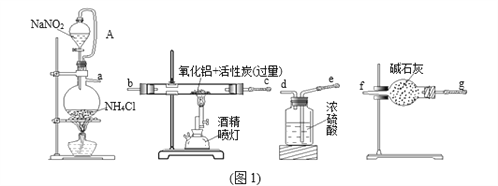
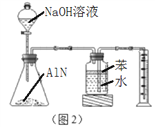
题目内容
【题目】25℃时,向50mL 0.018mol/L![]() 溶液中加入50mL 0.02mol/L盐酸生成沉淀。已知:
溶液中加入50mL 0.02mol/L盐酸生成沉淀。已知: ![]() ,则生成沉淀后的体系中
,则生成沉淀后的体系中![]() 为(忽略溶液体积变化)
为(忽略溶液体积变化)
A. ![]() mol/L B.
mol/L B. ![]() mol/L
mol/L
C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
【答案】A
【解析】n(AgNO3)=0.018mol/L![]() 0.05L=9
0.05L=9![]() 10-4mol,n(HCl)=0.02mol/L
10-4mol,n(HCl)=0.02mol/L![]() 0.05L=1
0.05L=1![]() 10-3mol,AgNO3与HCl反应的方程式为AgNO3+HCl=AgCl↓+HNO3,反应后HCl过量,n(HCl)余=1
10-3mol,AgNO3与HCl反应的方程式为AgNO3+HCl=AgCl↓+HNO3,反应后HCl过量,n(HCl)余=1![]() 10-3mol-9
10-3mol-9![]() 10-4mol=1
10-4mol=1![]() 10-4mol,此时c(Cl-)=1
10-4mol,此时c(Cl-)=1![]() 10-4mol
10-4mol![]() (0.05L+0.05L)=1
(0.05L+0.05L)=1![]() 10-3mol/L,Ksp(AgCl)=c(Ag+)c(Cl-),c(Ag+)=1.8
10-3mol/L,Ksp(AgCl)=c(Ag+)c(Cl-),c(Ag+)=1.8![]() 10-10
10-10![]() (1
(1![]() 10-3)=1.8
10-3)=1.8![]() 10-7(mol/L),答案选A。
10-7(mol/L),答案选A。

练习册系列答案
相关题目
【题目】常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | Na2CO3 | 稀盐酸 |
③ | CO2 | Na2O2 | H2O |
④ | FeCl3溶液 | Cu | 稀硫酸 |
A. ①③B. ①④C. ②④D. ②③
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A. 反应达到平衡时,X的转化率为50%
B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C. 增大X浓度使平衡向生成Z的方向移动,X体积分数减小
D. 改变温度可以改变此反应的平衡常数