题目内容
【题目】焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染等方面应用广泛。利用SO2生产Na2S2O5的工艺如图:
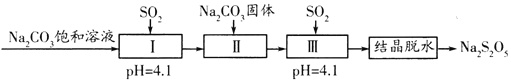
资料:Na2S2O5通常是由NaHSO3过饱和溶液经结晶脱水制得,下列说法正确的是( )
A.Na2S2O5是Na2SO3和SO2的混合物
B.pH=4.1时,I中主要反应的化学方程式为Na2CO3+SO2=Na2SO3+CO2
C.加入Na2CO3固体的目的是调节pH,促进Ⅲ中SO2的再吸收
D.“结晶脱水”过程中反应的化学方程式为2NaHSO3=Na2S2O5+H2O
【答案】CD
【解析】
由流程可知,I中发生Na2CO3+2SO2+H2O=2NaHSO3+CO2,加入Na2CO3固体,并再次充入SO2,可得到NaHSO3过饱和溶液,NaHSO3过饱和溶液经结晶脱水制得Na2S2O5。
A.Na2S2O5为纯净物,由NaHSO3过饱和溶液经结晶脱水制得,故A错误;
B.Na2SO3溶液呈碱性,①Ⅰ中反应的化学方程式为Na2CO3+2SO2+H2O=2NaHSO3+CO2,故B错误;
C.工艺中加入Na2CO3固体,并再次充入SO2的目的是调节pH,促进Ⅲ中SO2的再吸收,得到NaHSO3过饱和溶液,故C正确;
D.由题给信息可知Na2S2O5通常是由NaHSO3过饱和溶液经结晶脱水制得,则反应的化学方程式为2NaHSO3=Na2S2O5+H2O,故D正确。
故选:CD。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.40 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是( )
A.根据实验①、②可以推测该反应正反应△H>0
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
【题目】根据下列操作及现象,所得结论不正确的是![]()
![]()
序号 | 操作及现象 | 结论 |
A | 将 |
|
B | “ |
|
C | 向25mL冷水和沸水中分别滴入5滴 | 温度升高, |
D | 将固体 | 同温下溶解度:
|
A. A B. B C. C D. D