题目内容
1.化学与人类生产、生活,社会可持续发展密切相关,下列说法正确的是( )| A. | 用厨房垃圾发酵制沼气属于物理变化 | |
| B. | 可用水作镁铝合金爆炸时的灭火剂 | |
| C. | 推广使用煤液化技术科减少温室气体二氧化碳的排放 | |
| D. | 超导材料K3C60在熔融状态下能够导电,说明K3C60是电解质 |
分析 A.沼气的主要成分是甲烷,是不同于厨房垃圾的新物质;
B.镁能与热水反应生成氢气;
C.煤液化,是把固体炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术;
D.电解质是指溶于水溶液中或在熔融状态下就能够导电(电解离成阳离子与阴离子)的化合物.
解答 解:A.沼气的主要成分是甲烷,是不同于厨房垃圾的新物质,属化学变化,故A错误;
B.镁能与热水反应生成氢气,不能做灭火剂,故B错误;
C.煤液化,是把固体炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术,但二氧化碳排放,故C错误;
D.K3C60是化合物,它在熔融状态下能够电离出自由移动的离子能够导电,是电解质,故D正确.
故选D.
点评 本题考查较为综合,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养,提高学生学习的积极性,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
20.下列物质的结构或性质与氢键无关的是( )
| A. | 乙醚的沸点 | B. | 乙醇在水中的溶解度 | ||
| C. | 氢化镁的晶格能 | D. | DNA的双螺旋结构 |
9.X、Y、M、N是短周期主族元素,且原子序数依次增大.已知X原子的最外层电子数是电子层数的3倍,X、M同主族,Y原子在短周期主族元素中原子半径最大.下列说法不正确的是( )
| A. | M与X的化合物对应的水化物不一定都是强酸 | |
| B. | Y2X和Y2X2中化学键类型相同,阴、阳离子的个数比相同 | |
| C. | 气态氢化物的热稳定性:M<N | |
| D. | 离子半径r:r(X2-)>r(Y+) |
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、Cl-、NO3-、K+ | |
| B. | 滴入酚酞显红色的溶液中:Na+、Al3+、CO32-、AlO2- | |
| C. | 加入铝粉产生H2的溶液中:Fe2+、Na+、SO42-、ClO- | |
| D. | 0.1mol•L-1 NaHCO3溶液中:Na+、NH4+、SO42-、NO3- |
6.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 17.6 g丙烷中所含的共价键数目为4NA | |
| B. | 常温下,1L pH=13的Ba(OH)2溶液中含有的OH-离子数目为0.2NA | |
| C. | 标准状况下,5.6 L NO和5.6 L O2混合后的分子总数目为0.5NA | |
| D. | 电解精炼铜时,若阳极质量减少64 g,则阴极得到电子的数目为2NA |
10.某同学利用锌、氧化铜和稀硫酸制取铜,他设计了两套方案,
方案Ⅰ:利用锌与足量稀硫酸反应制氢气,氢气还原氧化铜;
方案Ⅱ:氧化铜溶于稀硫酸生成硫酸铜,然后用锌与硫酸铜反应制备铜.
下列关于方案Ⅰ和Ⅱ的评价不正确的是( )
方案Ⅰ:利用锌与足量稀硫酸反应制氢气,氢气还原氧化铜;
方案Ⅱ:氧化铜溶于稀硫酸生成硫酸铜,然后用锌与硫酸铜反应制备铜.
下列关于方案Ⅰ和Ⅱ的评价不正确的是( )
| A. | 方案Ⅱ比方案Ⅰ操作简便 | |
| B. | 等质量的锌,相同条件下方案Ⅰ和方案Ⅱ中制得的铜的质量相同 | |
| C. | 等质量的H2SO4参加反应,方案Ⅰ制取铜的质量比方案Ⅱ的少 | |
| D. | 为了加快锌与稀硫酸反应,可以在溶液中加入少量氧化铜 |
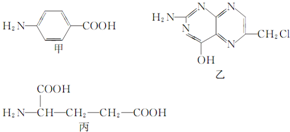 叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成.
叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成.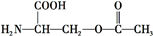 .
.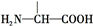
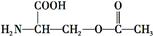 +2NaOH→HOCH2CH(NH2)COONa+H2O+CH3COONa.
+2NaOH→HOCH2CH(NH2)COONa+H2O+CH3COONa.