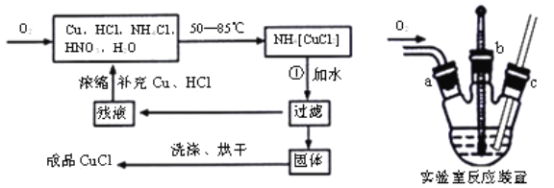
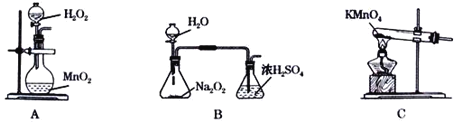
题目内容
【题目】室温下,用0.100mol/L NaOH溶液分别滴定20.00mL 0.100mol/L的盐酸和醋酸。下列说法正确的是
A.起始时盐酸和醋酸溶液的pH相同
B.V(NaOH)=10.00mL时,醋酸溶液中,![]()
C.恰好中和时,两种酸所用NaOH溶液体积不相等,醋酸用的体积少
D.V(NaOH)=20.00mL时,c(Cl-)>c(CH3COO-)
【答案】D
【解析】
A.醋酸是弱电解质,部分电离,0.100 mol/L的盐酸和醋酸,后者的pH大,A选项错误;
B.V(NaOH)=10.00mL时,氢氧化钠滴定醋酸的溶液中的溶质为等物质的量的CH3COOH和CH3COONa,CH3COOH的电离大于CH3COO-的水解,![]() ,B选项错误;
,B选项错误;
C.醋酸是弱电解质,部分电离,因此恰好中和时,两种酸所用NaOH溶液体积不相等,醋酸用的体积更多,C选项错误;
D.V(NaOH)=20.00mL时,两溶液中的溶质分别是NaCl和CH3COONa,且二者的物质的量相等,考虑CH3COO-水解,故c(Cl-)>c(CH3COO-),D选项正确;
答案选D。

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目