题目内容
【题目】(1)指出下列能量的变化:(每空1分)
学校燃烧煤煮饭 ,用畜电池点亮灯泡 。
(2)原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计如图装置:
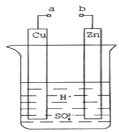
①a和b不连接时,烧杯中现象是 。
②a和b用导线连接,Cu极为原电池___极(填“正”或“负”),电极反应式为: ;溶液中H+移向_____(填“Cu”或“Zn”)极。电池总反应式为: 。
③若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为_ ___g。
【答案】(1) 化学能转化为热能 、电能转化为光能 (2) ① 锌片逐渐溶解,锌片上有气泡冒出
②正;2H++2e-=H2↑;Cu; ③Zn+H2SO4=ZnSO4+H2↑ ;21.6
【解析】
试题分析:(1)学校燃烧煤煮饭属于化学能转化为热能;用畜电池点亮灯泡属于电能转化为光能。
(2)①a和b不连接时,铜和稀硫酸不反应,锌与稀硫酸反应生成硫酸锌和氢气,则烧杯中现象是锌片逐渐溶解,锌片上有气泡冒出。
②a和b用导线连接后构成原电池,锌的金属性强于铜,则锌是负极,铜是正极,溶液中的氢离子在正极放电,则正极电极反应式为2H++2e-=H2↑;溶液中H+移向Cu极。电池总反应式为Zn+H2SO4=ZnSO4+H2↑。
③若电解质溶液改为AgNO3溶液,正极是溶液中的银离子放电,电极反应式为Ag++e-=Ag,当转移0.2mol电子时,正极析出0.2mol,因此理论上Cu片质量变化为0.2mol×108g/mol=21.6g。

【题目】(1)元素周期表分为 个横行,即 个周期,周期表中有 个纵行,共 个族。(每空1分)
(2)写出下列物质的电子式:①CO2 ;②NaOH 。(每空2分)
(3)下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:(离子方程式2分,其余每空1分)
主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
① 在这些元素中最活泼的非金属元素是 。
② 元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 。
③ 呈两性的氢氧化物是 ,其与③的最高价氧化物水化物反应的离子方程式为 。
④ 在③~⑦元素中,原子半径最大的是 。