题目内容
根据氧化还原反应Cu+2Ag+═Cu2++2Ag设计一个原电池?并判断正负极、写出各电极电极反应方程和反应的类型(在方框内画出原电池装置图)


根据电池反应式知,铜易失电子作负极,银离子得电子发生还原反应,则银作正极,铜电极对应的电解质溶液为可溶性的铜盐,银电极对应的电解质溶液为可溶性的银盐溶液,铜电极上电极反应式为Cu-2e-=Cu2+,
正极上银离子得电子发生还原反应,电极反应式为Ag++e-=Ag,所以其装置图为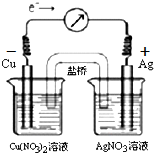
,答:正极银,负极铜;负极:Cu-2e-=Cu2+,正极Ag++e-=Ag;氧化反应,还原反应;装置图为 .
.
正极上银离子得电子发生还原反应,电极反应式为Ag++e-=Ag,所以其装置图为

,答:正极银,负极铜;负极:Cu-2e-=Cu2+,正极Ag++e-=Ag;氧化反应,还原反应;装置图为
 .
.
练习册系列答案
相关题目
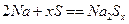 。但工作温度过高是这种高性能电池的缺陷。科学家研究发现,采用多硫化合物[如
。但工作温度过高是这种高性能电池的缺陷。科学家研究发现,采用多硫化合物[如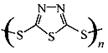 ]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列关于此种多硫化合物的叙述正确的是
]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列关于此种多硫化合物的叙述正确的是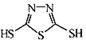 转化为
转化为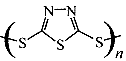 t的过程
t的过程 [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
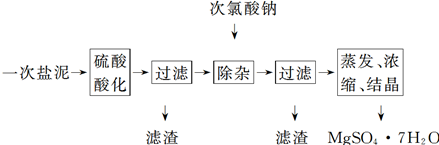
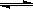 CO2(g) + H2(g),得到如下三组数据:
CO2(g) + H2(g),得到如下三组数据: