��Ŀ����
������ʵĵ���ƽ�⡢�����ˮ��ƽ�����������ܽ�ƽ������ڻ�ѧƽ�⡣
��֪H2A��ˮ�д�������ƽ�⣺H2A=H����HA����HA�� H����A2����
H����A2����
(1)������NaHA��Һ��pH________(����ţ���ͬ)��ԭ����_____________��
A������7������������ B��С��7 C������7 D����ȷ��
(2)ij�¶��£�����0.1 mol��L��1��NaHA��Һ����εμ�0.1 mol��L��1 KOH��Һ����Һ������(���Ի�Ϻ���Һ������仯)����ʱ�û����Һ�е����й�ϵһ����ȷ����________��
A��c(H��)��c(OH��)��1.0��10��14
B��c(Na��)��c(K��)��c(HA��)��2c(A2��)
C��c(Na��)>c(K��)
D��c(Na��)��c(K��)��0.05 mol��L��1
(3)��֪������H2A�ĸ���(CaA)�ı�����Һ�д�������ƽ�⣺CaA(s)??Ca2��(aq)��A2��(aq)����H>0����Ҫʹ����Һ��Ca2��Ũ�ȱ�С���ɲ�ȡ�Ĵ�ʩ��________��
A�������¶ȡ����������� B�������¶�
C������NH4Cl���� D������Na2A����
��(1)B��HA��ֻ���벻ˮ�⣬������
(2)BC��(3)BD
����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�ij��Ԫ��(��H2A��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�H2A=H����HA����HA�� H����A2�����ش��������⣺
H����A2�����ش��������⣺
(1)NaHA��Һ________(������ԡ������Լ��ԡ����������ԡ����������ȷ����)��ԭ����______________________��
(2)ij�¶��£���0.1 mol��L��1��NaHA��Һ�е���0.1 mol��L��1 KOH��Һ�����ԣ���ʱ��Һ�����¹�ϵһ����ȷ����________(����ĸ)��
| A��c(H��)��c(OH��)��1��10��14 mol��L��1 |
| B��c(Na��)��c(K��)��c(HA��)��2c(A2��) |
| C��c(Na��)>c(K��) |
| D��c(Na��)��c(K��)��0.05 mol��L��1 |
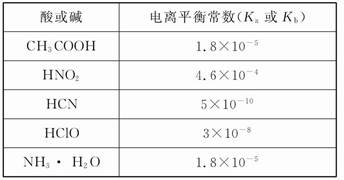
25 ��ʱ,����ƽ�ⳣ��:
| ����Ļ�ѧʽ | CH3COOH | HClO | H2CO3 |
| ����ƽ�ⳣ��(25 ��) | 1.8��10-5 | 3.0�� | K1=4.3��10-7 K2=5.6��10-11 |
�ش���������:
(1)���ʵ���Ũ��Ϊ0.1 mol/L��������������:
a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;
pH�ɴ�С��˳��������������������(����)��
(2)������0.1 mol/L��CH3COOH��Һ��ˮϡ������,���б���ʽ������һ����С������������;
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)��c(OH-) D.c(OH-)/c(H+)
(3)���Ϊ10 mL pH=2�Ĵ�����Һ��һԪ��HX�ֱ��ˮϡ����1 000 mL,ϡ����pH�仯��ͼ,��HX�ĵ���ƽ�ⳣ����������(����ڡ��������ڡ���С�ڡ�)�����ƽ�ⳣ��;�������� ��,
ϡ�ͺ�,HX��Һ��ˮ���������c(H+)��������(����ڡ��������ڡ���С�ڡ�)������Һ��ˮ���������c(H+),�������� ;

(4)25 ��ʱ,CH3COOH��CH3COONa�Ļ����Һ,����û��ҺpH=6,����Һ��c(CH3COO-)-c(Na+)=������������������������(��ȷ��ֵ)��
(1)��25 ��ʱ,��20 mL 0.1 mol��L-1 CH3COOH��Һ��20 mL 0.1 mol��L-1 HSCN��Һ�ֱ���20 mL 0.1 mol��L-1 NaHCO3��Һ���,ʵ���ò������������(V)��ʱ��(t)�ı仯��ͼ��ʾ����Ӧ��ʼ��������Һ����CO2��������ʴ������Բ����ԭ�������������������������������������� 
��Ӧ��������������Һ��,c(CH3COO-)��������c(SCN-)(�>����<����=��)��
���������¶Ȳ���,�ڴ�����Һ�м�����������,���������С������������(�����)��
| A��c(CH3COO-) | B��c(H+) | C��KW | D���������ƽ�ⳣ�� |

(2)��ͼΪij�¶���,PbS(s)��ZnS(s)��FeS(s)�ֱ�����Һ�дﵽ�����ܽ�ƽ���,��Һ��S2-Ũ�ȡ�����������Ũ�ȱ仯�������������ֳ����м�����,�����ܽ������������(�ѧʽ)���������ɵ�ZnS��Һ�е�����������ͬŨ�ȵ�Pb2+��Fe2+����Һ,��,ZnS������ת��Ϊ��������(�ѧʽ)������

(3)��֪������һ�ֶ�Ԫ����,��������(NaHC2O4)��Һ�����ԡ�������,��10 mL 0.01 mol��L-1 H2C2O4��Һ�еμ�10 mL 0.01 mol��L-1 NaOH��Һʱ,�Ƚ���Һ�и�������Ũ�ȵĴ�С��ϵ��������������������������������,c(H2C2O4)������c(C2
 )(�<����>����=��)��
)(�<����>����=��)�� ijͬѧ�ù�ҵ����ͭ�����������������ʣ��Ʊ�������CuSO4��5H2O��������������
�����ֲ����������ԣ���
I��ȡ��ҵ����ͭ���壬��ϡ�����ܽ⣬���ˡ�
II������Һ�еμ�H2O2��Һ���Լ��ȡ�
III����II����Һ�м���CuO��ĩ��pH��4��
IV��������У����ˣ���Һ��ϡ�����ữ��pH��1��
V������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����þ��塣
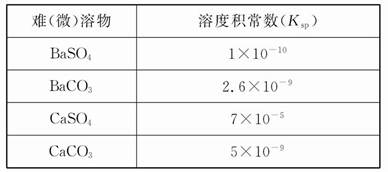
��֪�����������������������pH��Ksp��25�棩���±���
| ���� | Fe(OH)3 | Fe (OH)2 | Cu(OH)2 |
| ��ʼ����ʱpH | 2.7 | 7.6 | 4.7 |
| ��ȫ����ʱpH | 3.7 | 9.6 | 6.7 |
| Ksp | 4.0��10�C38 | 8.0��10�C16 | 2.2��10�C20 |
��1��II�з�����Ӧ�����ӷ���ʽ�� ��
��2��II�н�Fe2+����ΪFe3+��Ŀ���� ��
��3����K3[Fe(CN)6]�����軯�أ���֤II��Fe2+�Ƿ�ת����ȫ�������� ��
��4��III�з�����Ӧ�����ӷ���ʽ�� ��
ͨ������˵���ڴ������µ���Һ��Fe3+�Ƿ������ȫ________________________(��ʾ������Һ��ij����Ũ��С��1.0��10�C5 mol/Lʱ����Ϊ�����ӳ�����ȫ)��
��5��Ӧ�û�ѧƽ���ƶ�ԭ������IV�С���Һ��ϡ�����ữ����ԭ�� ��