题目内容
【题目】(1)第四周期中,未成对电子数最多的元素是________,(填名称)它位于第________族;核外电子排布式是__________________。它有________种运动状态不同的电子,其价电子排布图为:______________。
(2)已知NH5为离子化合物,写出其电子式:________。
(3)某同学根据掌握的知识分析Mg的核外电子排布为![]() 。该同学所画的电子排布图违背了________。
。该同学所画的电子排布图违背了________。
(4)在基态 14C原子中,核外存在________对自旋相反的电子。
【答案】铬 ⅥB 1s22s22p63s23p63d54s1或[Ar]3d54s1 24 ![]()
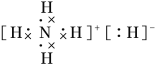 能量最低原理 2对
能量最低原理 2对
【解析】
(1)第四周期中未成对电子数最多的冤死,其核外电子排布式为1s22s22p63s23p63d54s1,有6个未成对电子,为24号元素,其名称是铬,位于第ⅥB族;在原子中,每一个电子的运动状态都是不一样的,铬原子核外有24个电子,因此它有24种运动状态不同的电子,其价电子排布图为:![]() ;
;
(2)NH5为离子化合物,由NH4+和H-构成,则其电子式为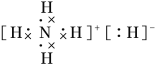 ;
;
(3)电子填充时,先填充能量较低的能级,3s能级的能量低于3p能量,因此电子应先填满3s能级,再填充3p能级,3s能级中应该有2个电子,而3p能级中没有电子,违反了能量最低原理;
(4)基态14C原子的核外电子排布图为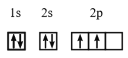 ,核外存在2对自旋相反的电子。
,核外存在2对自旋相反的电子。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】已知辉铜矿、软锰矿的主要成分如下表所示:
矿石 | 辉铜矿 | 软锰矿 |
主要成分 | Cu2S、Fe2O3、SiO2 | MnO2、SiO2 |
某化工厂拟以这两种矿石为原料采用湿法冶炼铜,工艺如下:
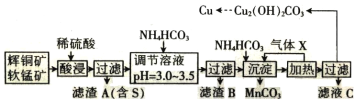
回答下列问题:
(1)气体 X 遇浓硝酸产生“白烟”,写出气体 X 的电子式:______________________________。
(2)提高“酸浸”速率的措施有______________________________(填两条)。
(3)用离子方程式表示“酸浸”中 MnO2 的作用:______________________________,被氧化的元素是______________________________(填元素符号)。
(4)已知 CH3COONH4 溶液呈中性,则常温下,NH4HCO3 溶液 pH______________________________(填“>”、“<”或“=”)7,理由是__________。
(5)从滤液 C 中可以提取一种化学肥料,它的化学式为_____________________________。
(6) 从溶液中析出的碱式碳酸铜可能带有结晶水,设其通式为 Cu2(OH)2CO3·xH2O。准确称取a g 样品,灼烧至恒重,称得 CuO 的质量,固体质量减轻 b g,则 x 为______________________________。
【题目】草酸合铁酸钾晶体Kx[Fe(C2O4)y]·3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程。
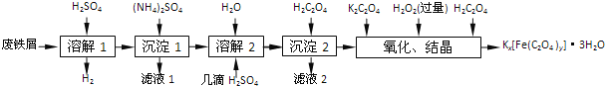
已知:(NH4)2SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
温度/℃ | 10 | 20 | 30 | 40 | 50 |
(NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
FeSO4·7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | ― |
(NH4)2SO4·FeSO4·6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)废铁屑在进行“溶解1”前,需用在5% Na2CO3溶液中加热数分钟,并洗涤干净。Na2CO3溶液的作用是________。
(2)“溶解1”应保证铁屑稍过量,其目的是___________。“溶解2”加“几滴H2SO4”的作用是________。
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、________、过滤、用乙醇洗涤、干燥。用乙醇洗涤的目的是____________。
(4)“沉淀”时得到的FeC2O4·2H2O沉淀需用水洗涤干净。检验沉淀是否洗涤干净的方法是_______。
(5)“结晶”应将溶液放在黑暗处等待晶体的析出,这样操作的原因是__________。
(6)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤[备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250 mL待测液。
步骤2:用移液管移取25.00 mL待测液于锥形瓶中,加入稀H2SO4酸化,_________,C2O42-转化为CO2被除去。
步骤3:向步骤2所得溶液中______________。
步骤4:用c mol·L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液。