题目内容
【题目】下列说法中错误的是( )
A.从 CH4、NH4+、SO42- 为正四面体结构,可推测 PH4+、PO43-也为正四面体结构
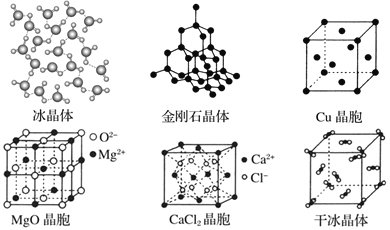
B.1 mol 金刚石晶体中,平均含有 2 mol C—C 键
C.碱金属单质的熔点从 Li 到 Cs 逐渐减小
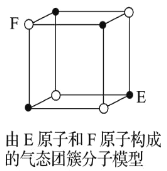
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为 EF 或 FE
【答案】D
【解析】
A.PH4+、PO43-分别是铵根和硫酸根的等电子体,根据等电子原理可知,这种两离子均为正四面体结构,故A正确;
B.金刚石晶体中,每个C原子与其它4个C原子形成共价键,且每2个C原子形成1个共价键,则1 mol金刚石晶体中,平均含有4mol×![]() =2 molC-C键,故B正确;
=2 molC-C键,故B正确;
C.碱金属都属于金属晶体,从Li到Cs金属阳离子半径增大,原子核对最外层电子吸引力减弱,金属键减弱,所以熔沸点降低,故C正确;
D.团簇分子中含有4个E、4个F原子,分子式应为E4F4或F4E4,故D错误;
答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目