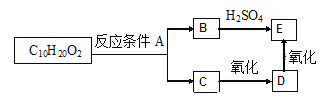
题目内容
【题目】硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)—炭粉还原法制备,原理为:Na2SO4+2CNa2S+2CO2↑。其主要流程如下:
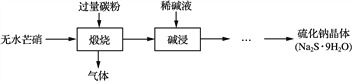
(1) 上述流程中采用稀碱液比用热水更好,理由是________________________________________________________________________。
(2) 已知:I2+2S2O32-===2I-+S4O62-。所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1 I2溶液滴定至终点,用去5.00 mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为____________。
②判断步骤c中滴定终点的方法为______________。
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数,写出计算过程__________。
【答案】 热水会促进Na2S水解,而稀碱液能抑制Na2S水解 ZnCO3+S2-===ZnS+CO 溶液由蓝色变为无色,且半分钟内不变色。 步骤b中消耗的I2有:
n(I2)=0.050 00 mol·L-1×5.00 mL×10-3 L·mL-1=2.500×10-4 mol
n(Na2S2O3·5H2O)=2n(I2)=5.000×10-4 mol(1分)
w(Na2S2O3·5H2O)=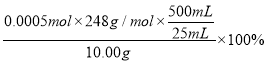
=24.8%(1分)
步骤c中,加入的I2有:
n(I2)=0.050 00 mol·L-1×50.00 mL×10-3 L·mL-1=2.500×10-3 mol(1分)
溶液中Na2S2O3消耗的I2有:2.500×10-4 mol(1分)
滴入的标准Na2S2O3溶液消耗多余的I2有:
15.00 mL×10-3 L·mL-1×0.100 0 mol·L-1×1/2=7.500×10-4 mol
溶液中Na2S有:
n(Na2S)=(2.500×10-3-2.500×10-4-7.500×10-4)mol=1.500×10-3 mol(1分)
w(Na2S·9H2O)=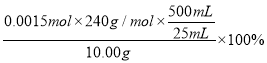
=72.0%(1分)
【解析】(1)硫化钠水解,溶液显碱性,水解吸热,热水会促进Na2S水解,而稀碱液能抑制Na2S水解。(2)①步骤b中用ZnCO3除去Na2S,反应中生成更难溶的ZnS,反应的离子方程式为 ZnCO3+S2-=ZnS+CO32-。②碘遇淀粉显蓝色,则判断步骤c中滴定终点的方法为溶液由蓝色变为无色,且半分钟内不变色。③步骤b中消耗的I2为:
n(I2)=0.050 00 mol·L-1×5.00 mL×10-3 L·mL-1=2.500×10-4 mol
n(Na2S2O3·5H2O)=2n(I2)=5.000×10-4 mol
w(Na2S2O3·5H2O)= =24.8%
=24.8%
步骤c中,加入的I2有:
n(I2)=0.050 00 mol·L-1×50.00 mL×10-3 L·mL-1=2.500×10-3 mol
溶液中Na2S2O3消耗的I2有:2.500×10-4 mol
滴入的标准Na2S2O3溶液消耗多余的I2有:
15.00 mL×10-3 L·mL-1×0.100 0 mol·L-1×1/2=7.500×10-4 mol
溶液中Na2S有:
n(Na2S)=(2.500×10-3-2.500×10-4-7.500×10-4)mol=1.500×10-3 mol
w(Na2S·9H2O)= =72.0%
=72.0%