题目内容
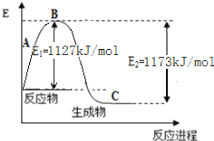
【题目】某反应过程能量变化如图所示,下列说法正确的是( )
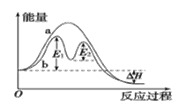
A.该反应为放热反应,热效应ΔH=E1-E2
B.有催化剂条件下,反应的活化能等于E1+E2
C.使用催化剂后,整个反应的速率快慢由E2对应反应决定
D.曲线b说明催化剂参与反应过程,降低反应的活化能,但不改变ΔH
【答案】D
【解析】
A、由图可知,反应物总能量高于生成物总能量,故该反应为放热反应,E1表示有催化剂条件下第一阶段反应的活化能,E2表示有催化剂条件下第二阶段反应的活化能,其热效应为ΔH![]() E1-E2,故A错误;
E1-E2,故A错误;
B、有催化剂条件下,反应的活化能应为能量较高的E1,故B错误;
C、因E1>E2,故使用催化剂后,整个反应的速率快慢由E1对应反应决定,故C错误;
D、催化剂能够降低化学反应的活化能,故曲线b说明催化剂参与反应过程,反应的ΔH只由物质的始终态有关,故ΔH不变,因此D正确。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】(1)实验测得5g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5 kJ的热量。试写出甲醇燃烧的热化学方程式:___________________________。
(2)现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意如图。根据下列已知键能数据计算N-H键键能为____________________kJ/mol 。
化学键 | H-H |
|
键能(kJ/mol) | 436 | 946 |
(3)用如图所示装置进行中和热测定实验,请回答下列问题:

仪器A的名称为 ________________________ 。
取30mLH2SO4(0.5mol·L-1)溶液与50mLNaOH(0.5mol·L-1)溶液在小烧杯中进行中和反应,三次实验温度平均升高4.1℃,已知中和后生成的溶液的比热容为![]() ,溶液的密度均为1g/cm3,通过计算可得中和热 ______ 。(保留小数点后一位)
,溶液的密度均为1g/cm3,通过计算可得中和热 ______ 。(保留小数点后一位)
上述实验数值结果与57.3kJ·mol-1有偏差,产生此偏差的原因可能是(填字母)______。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
实验中若改用60mLH2SO4(0.25mol·L-1)溶液与50mLNaOH(0.55 mol·L-1)溶液进行反应,与上述实验相比,所放出的热量 ______ (填“相等”、“不相等”),所求中和热 _____ (填“相等”、“不相等”),若用50mL0.5mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会 ______ (填“偏大”、“偏小”、“不受影响”)。