题目内容
【化学--选修:物质结构与性质】三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到.(1)写出制备 NF3的化学反应方程式:
(2)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是
(3)与铜属于同一周期,且未成对价电子数最多的元素基态原子核外电子排布式为
(4)理论上HF、NaAlO2和NaCl按6:1:2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,则该物质的化学式为
(5)根据下列四种元素的第一至第四电离能数据(单位:kJ?mol-1 ),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②T元素最可能是
分析:(1)根据反应物和生成物以及质量守恒定律可写出反应的化学方程式;
(2)NH3存在氢键,而NF3只存在分子间作用力,二者中NH3沸点较高;
(3)根据与铜在同一周期,且未成对价电子数最多,可推知外层价电子排布为3d54s1,应为Cr;
(4)根据题意可写出反应的化学方程式:6HF+NaAl02+2NaCl═2HCl+2H2O+Na3AlF6,Na3AlF6中心离子为Al,配位数为6;
(5)根据电离能的跳跃确定最外层有几个电子,然后根据得失电子规律,同一主族从上到下电离能依次递减,同一周期从左到右电离能依次递增,以此来确定在周期表中的位置.
(2)NH3存在氢键,而NF3只存在分子间作用力,二者中NH3沸点较高;
(3)根据与铜在同一周期,且未成对价电子数最多,可推知外层价电子排布为3d54s1,应为Cr;
(4)根据题意可写出反应的化学方程式:6HF+NaAl02+2NaCl═2HCl+2H2O+Na3AlF6,Na3AlF6中心离子为Al,配位数为6;
(5)根据电离能的跳跃确定最外层有几个电子,然后根据得失电子规律,同一主族从上到下电离能依次递减,同一周期从左到右电离能依次递增,以此来确定在周期表中的位置.
解答:解:(1)根据反应物和生成物以及质量守恒定律可知反应还应有NH4F生成,方程式为4NH3+3F2═NF3+3NH4F,
故答案为:4NH3+3F2═NF3+3NH4F;
(2)NH3存在氢键,而NF3只存在分子间作用力,两种作用力前者较强,物质的沸点较高,
故答案为:NH3能形成氢键,NF3只有范德华力;
(3)与铜在同一周期,且未成对价电子数最多,可推知外层价电子排布为3d54s1,应为Cr,原子序数为24,根据能量最低原理、构造原理、洪特规则可写出电子排布式为1s22s22p63s23p63d54s1,
故答案为:1s22s22p63s23p63d54s1(或[Ar]3d54s1);
(4)有题意可知该反应的化学方程式应为:6HF+NaAl02+2NaCl═2HCl+2H2O+Na3AlF6,该微溶物为:Na3AlF6,中心离子为Al,配位数为6,
故答案为:Na3AlF6;Al;6;
(5)①根据电离能的跳跃确定最外层有几个电子,表中R和U的第一电离能较小,但跳跃至第二电离能时突然变大,说明失去一个电子后变为稳定结构,最外层有一个电子,故R和U处于同族,
故答案为:R;U;
②由T元素电离能的变化可知T最外层有三个电子,位于周期表中第ⅢA族,在p区,若T为第二周期元素,应为B元素,E是第三周期元素中原子半径最小的元素,应为Cl元素,二者形成的化合物为BCl3,根据价层电子对模型可知应为平面正三角形结构,中心原子的杂化方式为sp2杂化,
故答案为:p;平面正三角形;sp2.
故答案为:4NH3+3F2═NF3+3NH4F;
(2)NH3存在氢键,而NF3只存在分子间作用力,两种作用力前者较强,物质的沸点较高,
故答案为:NH3能形成氢键,NF3只有范德华力;
(3)与铜在同一周期,且未成对价电子数最多,可推知外层价电子排布为3d54s1,应为Cr,原子序数为24,根据能量最低原理、构造原理、洪特规则可写出电子排布式为1s22s22p63s23p63d54s1,
故答案为:1s22s22p63s23p63d54s1(或[Ar]3d54s1);
(4)有题意可知该反应的化学方程式应为:6HF+NaAl02+2NaCl═2HCl+2H2O+Na3AlF6,该微溶物为:Na3AlF6,中心离子为Al,配位数为6,
故答案为:Na3AlF6;Al;6;
(5)①根据电离能的跳跃确定最外层有几个电子,表中R和U的第一电离能较小,但跳跃至第二电离能时突然变大,说明失去一个电子后变为稳定结构,最外层有一个电子,故R和U处于同族,
故答案为:R;U;
②由T元素电离能的变化可知T最外层有三个电子,位于周期表中第ⅢA族,在p区,若T为第二周期元素,应为B元素,E是第三周期元素中原子半径最小的元素,应为Cl元素,二者形成的化合物为BCl3,根据价层电子对模型可知应为平面正三角形结构,中心原子的杂化方式为sp2杂化,
故答案为:p;平面正三角形;sp2.
点评:本题考查物质结构与性质知识,涉及到电子排布式的书写、电离能等问题,做题时注意抓住题目提供的信息,以及利用电离能的跳跃值判断最外层电子数等问题;本题难度较大.

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
 【化学--选修3物质结构与性质】
【化学--选修3物质结构与性质】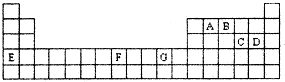
 该配离子中含有的化学键类型有
该配离子中含有的化学键类型有