题目内容
【题目】下列关于物质用途的叙述中,不正确的是( )
A.氨可用作制冷剂
B.可用铝制容器盛装浓盐酸
C.硅是太阳能电池的常用材料
D.铁红常用于制红色油漆和涂料
【答案】B
【解析】解:A.液氨气化吸热,能降温,所以氨可用作制冷剂,故A正确;B.氧化铝和Al均能和浓盐酸发生化学反应,因此不可用铝制容器盛装浓盐酸,故B错误;
C.硅常做半导体,可用于制造太阳能电池,故C正确;
D.氧化铁是红棕色的固体,常用于制造红色油漆和涂料,故D正确;
故选B.
A.液氨气化吸热,能环境降温;
B.氧化铝和Al均能和浓盐酸发生化学反应;
C.硅常做半导体,是制造太阳能电池的原料;
D.铁红的成分是氧化铁,是红棕色的固体.

 阅读快车系列答案
阅读快车系列答案【题目】利用下列装置可以完成的实验组合是
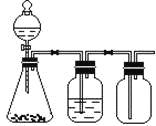
选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
C | Zn 稀硫酸 | 浓硫酸 | H2 |
D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
A. AB. BC. CD. D
【答案】B
【解析】
A. 二氧化锰与氯酸钾制取氧气,属于固体加热型,锥形瓶没有加热,所以不能用图中实验装置制取,选项A错误;
B.大理石与盐酸生成二氧化碳气体,属于固液常温型,盐酸有挥发性,挥发的HCl能与碳酸氢钠溶液反应产生二氧化碳气体,且二氧化碳密度比空气的大,能用向上排空气法收集;选项B正确。
C.锌粒与稀硫酸反应生成氢气,属于固液常温型,但氢气密度比空气的小,不能用向下排空气法收集,选项C错误;
D. 二氧化锰与浓盐酸制取氯气,属于固体加热型,锥形瓶没有加热,所以不能用图中实验装置制取,选项D错误;
故合理选项是B。
【题型】单选题
【结束】
20
【题目】下列物质中,不可作漂白剂的是( )
A. SO2 B. Ca(ClO)2 C. Na2SiO3 D. NaClO
【题目】雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法
(1)用活性炭还原法可以处理氨氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)![]() N2(g)+CO2(g) △H=Q kJ· mol-1。
N2(g)+CO2(g) △H=Q kJ· mol-1。
在T℃时,反应进行到不同时间测得各物质的浓度如下表。
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min 内,NO 的平均反应速率v(NO)=___________。
T1 ℃时,该反应的平衡常数K=___________。
②30min 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母)。___________。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min 后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5∶3 ∶3,则Q________0(填“>”、“=”或“<”)。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图甲所示。
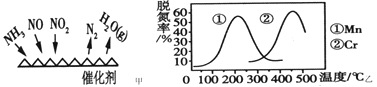
①由图甲可知,SCR技术中的氧化剂为___________。已知c(NO2)∶c(NO)=1∶1时脱氮效果最佳,若生成1mol N2时反应放出的热量为QkJ。此时对应的脱氮反应的热化学方程式为___________。
②图乙是不同催化剂Mn 和Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应的温度分别为________________。
【题目】碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是__________________。氯碱工业生产时,由于食盐水中通常含有少量NH4Cl,而在阳极区与生成的氯气反应产生少量NCl3,该反应的化学方程式为_____________。
(2)一定条件下,不同物质的量的CO2与不同体积的1.0mol/LNaOH溶液充分反应放出的热量如下表所示:
反应序号 | n (CO2)/mol | V (NaOH) /L | 放出的热量/kJ |
1 | 0.5 | 0.75 | a |
2 | 1.0 | 2.00 | b |
该条件CO2与NaOH 溶液反应生成NaHCO3的热化学反应方程式为______________________。
(3)利用CO可以将NO转化为无害的N2,其反应为: 2NO(g) +2CO(g) ![]() N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
N甲(CO)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
N乙(CO)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
/p>
①甲容器中,0~40min 内用NO的浓度变化表示的反应速率v(NO)=_____________。
②该反应的△H____0(填“>”或“<”)。
③甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡______(填“正向”、“逆向”或“不”)移动。
(4)常温下, 在(NH4)2C2O4溶液中,反应NH4++C2O42-+H2O![]() NH3·H2O+HC2O4-的平衡常数K=________________________。(已知常温下,NH3·H2O的电离平衡常数Kb=2×10-5,H2C2O4的电离平衡常数Ka1=5×10-2,Ka2=5×10-5)
NH3·H2O+HC2O4-的平衡常数K=________________________。(已知常温下,NH3·H2O的电离平衡常数Kb=2×10-5,H2C2O4的电离平衡常数Ka1=5×10-2,Ka2=5×10-5)
(5)在酸性电解质溶液中,以惰性材料作电极,将CO2转化为丙烯的原理如下图所示
①太阳能电池的负极是__________(填“a”或“b”)
②生成丙烯的电极反应式是_____________________________。