题目内容
【题目】雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法
(1)用活性炭还原法可以处理氨氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)![]() N2(g)+CO2(g) △H=Q kJ· mol-1。
N2(g)+CO2(g) △H=Q kJ· mol-1。
在T℃时,反应进行到不同时间测得各物质的浓度如下表。
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min 内,NO 的平均反应速率v(NO)=___________。
T1 ℃时,该反应的平衡常数K=___________。
②30min 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母)。___________。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min 后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5∶3 ∶3,则Q________0(填“>”、“=”或“<”)。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图甲所示。
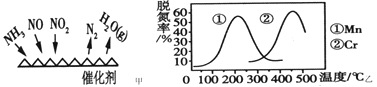
①由图甲可知,SCR技术中的氧化剂为___________。已知c(NO2)∶c(NO)=1∶1时脱氮效果最佳,若生成1mol N2时反应放出的热量为QkJ。此时对应的脱氮反应的热化学方程式为___________。
②图乙是不同催化剂Mn 和Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应的温度分别为________________。
【答案】 0.042 mol·L-1·min-1 9/16或0.5625 bc < NO、NO2 2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g) ΔH=-2Q kJ·mol-1 Mn、200 ℃ 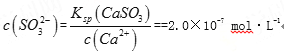
【解析】(1)分析图表数据,![]() 内,NO的平均反应速率
内,NO的平均反应速率![]() ,
,
化学平衡三段式列式计算平衡浓度:
![]()
![]() ;
;
起始量![]() 1 0 0
1 0 0
变化量![]() 0.6 0.3 0.3
0.6 0.3 0.3
平衡量![]() 0.4 0.3 0.3
0.4 0.3 0.3![]() ;
;
因此,本题正确答案是:0.042mol·L-1·min-1; 9/16或0.5625;
(2) 30min后,只改变某一条件,反应重新达到平衡,图表数据分析可以知道一氧化氮,氮气,二氧化碳浓度都增大;a.加入一定量的活性炭是固体,对平衡无影响,故a不符合;
b.通入一定量的NO,反应正向进行,达到平衡后一氧化氮、氮气、二氧化碳浓度增大,故b符合;c.适当缩小容器的体积,反应前后是气体体积不变的反应,平衡不动,但个物质浓度增大,符合要求,故c符合;d.加入合适的催化剂,只能改变化学反应速率,不能改变平衡,浓度不变,故d不符合;因此,本题正确答案是:bc;
(3)若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,![]() ,这说明升高温度平衡向逆反应方向移动,因此逆反应是吸热反应,则正反应是放热反应,故Q<,因此,本题正确答案是:<;
,这说明升高温度平衡向逆反应方向移动,因此逆反应是吸热反应,则正反应是放热反应,故Q<,因此,本题正确答案是:<;
(2)(1)由图甲可以知道SCR技术中NH3与NO、NO2反应产物为N2和水,故氧化剂为NO、NO2;脱氮效果最佳时C(NO2):C(NO)=1:1,因此反应的热化学方程式为. 2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g) ΔH=-2Q kJ·mol-1 ;因此,本题正确答案是: NO、NO2;. 2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g) ΔH=-2Q kJ·mol-1;
(2)根据图乙知Mn催化剂时,在![]() 左右脱氮率最高,Cr作催化剂,
左右脱氮率最高,Cr作催化剂,![]() 左右脱氮率最高,但二者的最高脱氮率差不多,使用Mn作催化剂需要的温度低,更经济,因此使用的最佳的催化剂和相应的温度分别为Mn、200 ℃左右;因此,本题正确答案是:Mn、200 ℃左右;
左右脱氮率最高,但二者的最高脱氮率差不多,使用Mn作催化剂需要的温度低,更经济,因此使用的最佳的催化剂和相应的温度分别为Mn、200 ℃左右;因此,本题正确答案是:Mn、200 ℃左右;
(3)根据硫酸钙的溶度积常数表达式![]() 可以知道,
可以知道, ,因此,本题正确答案是:
,因此,本题正确答案是:![]() .
.
点睛:解答要点:(1)分析图表数据结合化学反应速率概念计算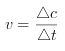 ,计算平衡浓度结合平衡常数概念是生成物浓度的幂次方乘积除以反应物的幂次方乘积得到;
,计算平衡浓度结合平衡常数概念是生成物浓度的幂次方乘积除以反应物的幂次方乘积得到;
(2)反应前后是气体体积不变的反应,图表数据分析可以知道一氧化氮,氮气,二氧化碳浓度都增大,说明改变的条件是缩小体积增大浓度,或加入一氧化氮达到新平衡后个物质浓度增大;(3)若![]() 后升高温度至
后升高温度至![]() ,达到平衡时,容器中NO、
,达到平衡时,容器中NO、![]() 、
、![]() 的浓度之比为
的浓度之比为![]() ,根据Qc与K的相对大小判断平衡移动方向,逆反应方向是吸热反应,正反应为放热反应;(2)(1)得电子化合价降低的反应物是氧化剂;(2)温度越高,对设备的要求越高,所以如果催化剂在较低温度下能较大程度的脱氢即可;根据生成
,根据Qc与K的相对大小判断平衡移动方向,逆反应方向是吸热反应,正反应为放热反应;(2)(1)得电子化合价降低的反应物是氧化剂;(2)温度越高,对设备的要求越高,所以如果催化剂在较低温度下能较大程度的脱氢即可;根据生成![]() 氮气放出QkJ热量,则生成
氮气放出QkJ热量,则生成![]() 氮气放出
氮气放出![]() 热量;(3)根据硫酸钙的溶度积常数表达式
热量;(3)根据硫酸钙的溶度积常数表达式![]() 进行计算;
进行计算;

 阅读快车系列答案
阅读快车系列答案【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:2SO2(g)+ O2(g)![]() 2SO3 △H<0。得到如表中的两组数据,下列说法不正确的是
2SO3 △H<0。得到如表中的两组数据,下列说法不正确的是
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
A. T1、T2的关系:T1 > T2
B. x= 1.6,y=0.2 ,t<6
C. K1、K2的关系:K2>K1
D. 实验1在前6min的反应速率υ(SO2)=0.2 mol·L-1·min-1