题目内容
【题目】某铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,及一定量的Fe2O3、MgO和CaO等。由该矿石制Co2O3的部分工艺流程如图:
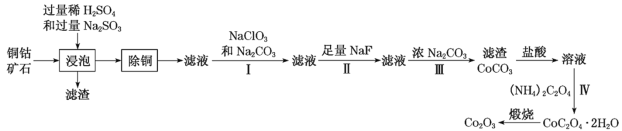
回答下列问题:
(1)“浸泡”过程中,钴(III)可转化为CoSO4,写出该转化的相关化学方程式:__。
(2)“除铜”若选用MnS,计算常温下该“除铜”反应的平衡常数K=__。[保留2位有效数字;已知常温下Ksp(MnS)=2.5×10–13,Ksp(CuS)=1.3×10–36]
(3)①步骤I中加入NaClO3与Fe2+反应的离子方程式为__。
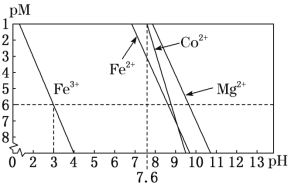
②常温下,溶液中金属离子(Mn+)的pM[pM=–lgc(Mn+)]随溶液pH变化关系如图所示,设加入NaClO3后,溶液中的c(Co2+)为0.1molL-1,依据如图分析,步骤I中加入Na2CO3调整溶液pH范围为__。[当c(Mn+)≤10–6molL–1,即认为该金属离子沉淀完全]
(4)步骤II中加入足量NaF的目的是__。
(5)过滤出的CoC2O42H2O固体经洗涤后,证明固体已洗净的操作为__。
(6)若某工厂用m1kg该铜钴矿石制备了m2kgCo2O3,假设产率为a,则该矿石中钴元素的百分含量为__。
【答案】2CoO(OH)+2H2SO4+Na2SO3=2CoSO4+Na2SO4+3H2O 1.9×1023 ClO![]() +6Fe2++6H+=Cl-+6Fe3++3H2O 3~7.6(或3≤pH<7.6) 形成沉淀,除去溶液中钙、镁离子 取少量最后一次洗涤液于试管中,加入硝酸酸化的硝酸银溶液,若无白色沉淀产生,则证明已洗净
+6Fe2++6H+=Cl-+6Fe3++3H2O 3~7.6(或3≤pH<7.6) 形成沉淀,除去溶液中钙、镁离子 取少量最后一次洗涤液于试管中,加入硝酸酸化的硝酸银溶液,若无白色沉淀产生,则证明已洗净 ![]() %
%
【解析】
铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,及一定量的Fe2O3、MgO和CaO等,由流程可知,加入过量稀硫酸和Na2SO3,可得Co2+、Cu2+、Fe2+、Mg2+、Ca2+,加入的Na2SO3主要是将Co3+、Fe3+还原为Co2+、Fe2+,加MnS可沉铜,然后加入NaClO3将Fe2+氧化为Fe3+,加入Na2CO3调pH,可以使Fe3+沉淀,过滤后所得滤液主要含有Co2+、Mg2+、Ca2+,再用NaF溶液除去钙、镁离子,过滤后,向滤液中加入浓Na2CO3溶液转为CoCO3固体,溶于盐酸后加入草酸铵溶液得到草酸钴晶体,煅烧后制得Co2O3。
(1)“浸泡”过程中,钴(III)可转化为CoSO4,该转化的相关化学方程式:2CoO(OH)+2H2SO4+Na2SO3=2CoSO4+Na2SO4+3H2O。故答案为:2CoO(OH)+2H2SO4+Na2SO3=2CoSO4+Na2SO4+3H2O;
(2)“除铜”若选用MnS,发生MnS+Cu2+![]() CuS+Mn2+,常温下该“除铜”反应的平衡常数K=
CuS+Mn2+,常温下该“除铜”反应的平衡常数K=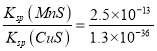 =1.9×1023,故答案为:1.9×1023;
=1.9×1023,故答案为:1.9×1023;
(3)①步骤I中加入NaClO3与Fe2+反应,生成Cl-和Fe3+,离子方程式为ClO![]() +6Fe2++6H+=Cl-+6Fe3++3H2O。故答案为:ClO
+6Fe2++6H+=Cl-+6Fe3++3H2O。故答案为:ClO![]() +6Fe2++6H+=Cl-+6Fe3++3H2O;
+6Fe2++6H+=Cl-+6Fe3++3H2O;
②设加入NaClO3后,溶液中的c(Co2+)为0.1molL-1,依据如图分析,pH>3时Fe3+完全沉淀,使CO2+不转化为沉淀,pH<7.6即可,步骤I中加入Na2CO3调整溶液pH范围为3~7.6(或3≤pH<7.6)。[当c(Mn+)≤10–6molL–1,即认为该金属离子沉淀完全]。故答案为:3~7.6(或3≤pH<7.6);
(4)步骤II中加入足量NaF的目的是形成沉淀,除去溶液中钙、镁离子。故答案为:形成沉淀,除去溶液中钙、镁离子;
(5)过滤出的CoC2O42H2O固体经洗涤后,检验洗涤液是否含有Cl-,证明固体已洗净的操作为:取少量最后一次洗涤液于试管中,加入硝酸酸化的硝酸银溶液,若无白色沉淀产生,则证明已洗净。故答案为:取少量最后一次洗涤液于试管中,加入硝酸酸化的硝酸银溶液,若无白色沉淀产生,则证明已洗净;
(6)若某工厂用m1kg该铜钴矿石制备了m2kg Co2O3,假设产率为a,设该矿石中钴元素的百分含量为x,由原子守恒可知m1kg×x×a×![]() =m2kg,解得x=
=m2kg,解得x=![]() %。故答案为:
%。故答案为:![]() %。
%。

【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
【题目】已知常温下浓度为0.1mol/L的几种溶液的pH如右下表。下列有关说法正确的是( )
溶质 | pH |
NaF | 7.5 |
Na2CO3 | 11.6 |
NaClO | 9.7 |
NaHCO3 | 8.3 |
A. 同温度同浓度下,酸由强到弱的顺序为:HF>H2CO3>HClO
B. 水解方程式:F-+H2O![]() HF+OH-的平衡常数为1×10-13
HF+OH-的平衡常数为1×10-13
C. 将CO2通入0.lmol/LNa2CO3溶液至溶液呈中性,则溶液中:2c(CO32-)+c(HCO3-)=0.1mol/L
D. 等物质的量的NaF和HF混合溶液中粒子浓度大小关系为:c(HF)>c(Na+)>c(F-)>c (H+)>c(OH-)