题目内容
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
| A.c(NH4+):③ > ② |
| B.pH:① > ② > ③ |
C.Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s) Mg2+ (aq) + 2OH- (aq)向溶解方向移动 Mg2+ (aq) + 2OH- (aq)向溶解方向移动 |
| D.等体积①和③混合溶液中 c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) |
D
试题分析:A、NH4Cl溶液和醋酸铵溶液均存在NH4+水解,但醋酸铵溶液中还存在醋酸根的水解,促进NH4+水解,导致c(NH4+):③ <②,错误;B、pH:① < ②< ③,错误;C、由题意知,Mg(OH)2溶于②的主要原因是由于NH4+与Mg(OH)2(s)溶解产生的OH-反应生成一水合氨,使OH-浓度降低,导致平衡Mg(OH)2(s)
 Mg2+ (aq) + 2OH- (aq)向溶解方向移动,错误;D、等浓度、等体积盐酸和醋酸铵溶液混合,二者恰好完全反应生成醋酸和氯化铵,且二者浓度相等均为3mol/L,溶液显酸性,c(H+) >c(OH-),NH4+水解消耗一部分,c(Cl-) >c(NH4+) ,H+来自醋酸的电离NH4+水解,c(H+) > c(CH3COO-)电离和水解是微弱的,c(NH4+) > c(H+),综上所述溶液中 c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) ,正确。
Mg2+ (aq) + 2OH- (aq)向溶解方向移动,错误;D、等浓度、等体积盐酸和醋酸铵溶液混合,二者恰好完全反应生成醋酸和氯化铵,且二者浓度相等均为3mol/L,溶液显酸性,c(H+) >c(OH-),NH4+水解消耗一部分,c(Cl-) >c(NH4+) ,H+来自醋酸的电离NH4+水解,c(H+) > c(CH3COO-)电离和水解是微弱的,c(NH4+) > c(H+),综上所述溶液中 c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) ,正确。
练习册系列答案
相关题目
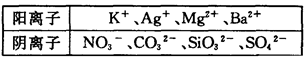
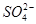 、
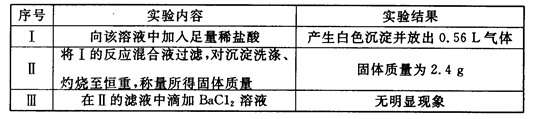
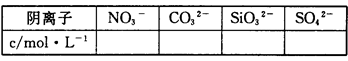
、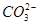 、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中