题目内容
下列各微粒的电子排布式或电子排布图正确的是( )
分析:能量最低原理:原子核外电子先占有能量较低的轨道.然后依次进入能量较高的轨道;
泡利原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态相同,③全空、全满或半满时能量最低;
根据以上规则分析.
泡利原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态相同,③全空、全满或半满时能量最低;
根据以上规则分析.
解答:解:A.2p能层有2个电子,应在2个不同的轨道,而且自旋状态相同,所以不符合洪特规则,故A错误;
B.Cr为24号元素,其原子的核外有24个电子,其电子排布式为1s22s22p63s23p63d54s1,符合基态电子排布规律,故B正确;
C.根据泡利原理,每个原子轨道上最多只能容纳2个自旋状态相反的电子,所以1s和2s轨道上的2个电子自旋状态应该相反,故C错误;
D.Br为35号元素,其原子的核外有35个电子,核外电子排布式为:1s22s22p63s23p63d104s24p5,故D错误;
故选B.
B.Cr为24号元素,其原子的核外有24个电子,其电子排布式为1s22s22p63s23p63d54s1,符合基态电子排布规律,故B正确;
C.根据泡利原理,每个原子轨道上最多只能容纳2个自旋状态相反的电子,所以1s和2s轨道上的2个电子自旋状态应该相反,故C错误;
D.Br为35号元素,其原子的核外有35个电子,核外电子排布式为:1s22s22p63s23p63d104s24p5,故D错误;
故选B.
点评:本题考查了基态原子的核外电子排布式和电子排布图,根据能量最低原理、泡利原理和洪特规则分析,题目难度一般.

练习册系列答案
相关题目
 《物质结构与性质》
《物质结构与性质》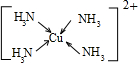
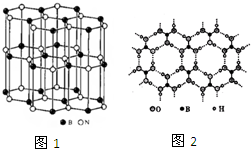 尿素(
尿素(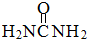 )和硼砂(Na2B4O7)在高温高压下反应可以获得硼氮化合物:
)和硼砂(Na2B4O7)在高温高压下反应可以获得硼氮化合物:


 键的数目之比为
。
键的数目之比为
。