题目内容
已知元素A、B、C、D、E、F均属前四周期,且原子序数依次增大, A的p能级电子数是s能级电子数的一半,C的基态原子2p轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能级层均排满,且最外层电子数为1。请回答下列问题:
(1)C原子基态时的电子排布式为?????????????? 。?
(2)B、C两种元素第一电离能为:????? ﹥ ???????? (用元素符号表示)。
试解释其原因: ??????????????????????????????????????????????????????? 。
(3)任写一种与AB- 离子互为等电子体的微粒????????????????????????????????? 。
(4)B与C形成的四原子阴离子的立体构型为??????????? ,其中B原子的杂化类型是???????? 。
(5)D和E形成的化合物的晶胞结构如图,其化学式为???????? ,E的配位数是??????????????? ;已知晶体的密度为? ρ g·cm-3,阿伏加德罗常数为NA,则晶胞边长a=??????????? cm.(用含 、NA的计算式表示)
、NA的计算式表示)

(1)1s22s22p4;(2)N>O;氮原子核外2p亚层处于半充满的较稳定结构,不易失去电子,故第一电离能比氧原子大;(3)CO或C22- 或O22+;(4)平面三角形,sp2;(5)CaF2,8,? 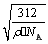 。
。
【解析】
试题分析:根据题意知,元素A、B、C、D、E、F均属前四周期,且原子序数依次增大, A的p能级电子数是s能级电子数的一半,A的原子核外电子排布式为1s22s22p2,则A为碳元素;C的基态原子2p轨道有2个未成对电子,C的原子核外电子排布式为1s22s22p4,则C为氧元素;又A、B、C原子序数依次增大,则B为氮元素;C与D形成的化合物中C显正化合价,则D为氟元素;E的M层电子数是N层电子数的4倍,则E为钙元素;F的内部各能级层均排满,且最外层电子数为1,则F为铜元素。(1)C为氧元素,原子基态时的电子排布式为1s22s22p4;(2)B为氮元素,C为氧元素,氮原子核外2p亚层处于半充满的较稳定结构,不易失去电子,两种元素第一电离能为N>O;(3)根据等电子体概念知,与CN-离子互为等电子体的微粒为CO或C22- 或O22+;(4)根据价层电子对互斥理论判断,B与C形成的四原子阴离子NO3—的立体构型为平面三角形,其中B原子的杂化类型是sp2;(5)利用切割法结合化合物的晶胞判断,其化学式为CaF2,E的配位数是8;由化合物CaF2的晶胞结构可知,1个晶胞中含有钙离子数目为8×1/8+6×1/2=4,含有氟离子数目为8,所以1mol晶胞的质量为312g,又晶体的密度为ρ g·cm-3,则1个晶胞的体积312/ρNAcm3,则晶胞边长a=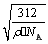 cm。
cm。
考点:考查物质结构与性质,涉及元素推断,元素周期律,第一电离能,核外电子排布式,分子空间构型及晶胞计算。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案 和○代表两种不同的粒子.E与D形成的化合物的晶胞是下列中的
和○代表两种不同的粒子.E与D形成的化合物的晶胞是下列中的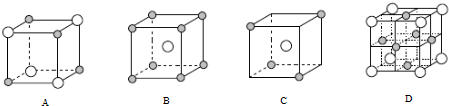

 和
和 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。