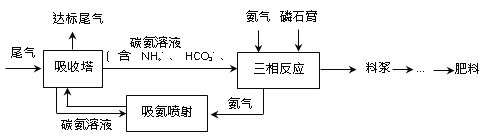
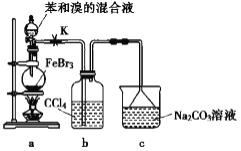
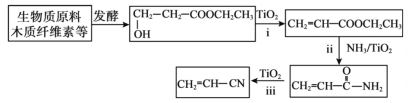
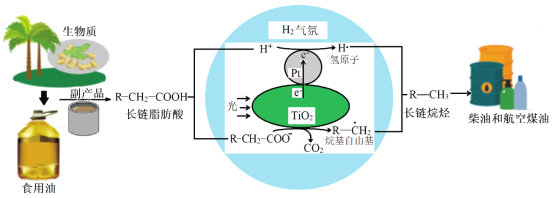
��Ŀ����
����Ŀ��Ϊ����ij�ӵ�ʳ�����Ƿ���KIO3��ȡ��ͬʳ����Ʒ�����±���ʾʵ�飺
����֪��KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O��
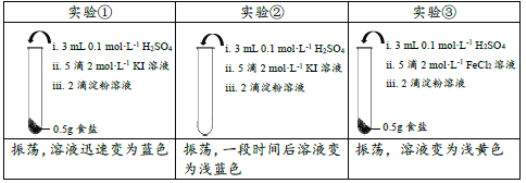
����˵���в���ȷ���ǣ� ��
A.����ʵ��ٲ���֤��ʳ����Ʒ�д���KIO3
B.ʵ����з�����Ӧ�����ӷ���ʽΪ4I-+O2+4H+=2I2+2H2O
C.ʵ�����Һ���ɫ��������Fe3+��֤��ʳ����Ʒ�д���KIO3
D.���ʵ��ٺ͢ڵ�������죬�����ƶ�ʵ����Ʒ�д���KIO3
���𰸡�C
��������
A��KI��Һ��Ҳ�е�Ԫ�أ���Һ����������KI�еĵ�Ԫ�ر����������˵ⵥ�ʣ����Խ���ʵ��ٲ���֤��ʳ����Ʒ�д���KIO3����A��ȷ��
B��ʵ�������Һ��Ϊdz��ɫ������Ԫ���غ��֪KI��Һ�еĵ����������Ի����±������ˣ����ǵ������������������ԣ�Ӧ�������������������ݵ����غ��Ԫ���غ�ɵ����ӷ���ʽΪ4I-+O2+4H+=2I2+2H2O����B��ȷ��
C��ʵ��۵�dz��ɫ�������ӵ���ɫ�����������ӱ������������Ľ��������������һ����KIO3��Ҳ�����ǿ����е���������C����
D���Ա�ʵ��ٺ͢ڵ���������֪ʵ����������Ի����·�����Ӧ��KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O����ҺѸ�ٱ�������ɫ��ʵ���Ҫ������ƶ�ʵ����Ʒ�д���KIO3����D��ȷ��
�ʴ�ΪC��

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
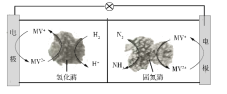
�Ƹ������������ϵ�д�����Ŀ����ˮ�Ȼ���![]() �ڵ��Ӽ����;�ϸ������������ҪӦ�á�һ���ɴ��̷�(��Ҫ����ΪFe��Ni��Pb�Ƚ�������)�Ʊ���ˮ�Ȼ��̵Ĺ�������(���ֲ�����������)��
�ڵ��Ӽ����;�ϸ������������ҪӦ�á�һ���ɴ��̷�(��Ҫ����ΪFe��Ni��Pb�Ƚ�������)�Ʊ���ˮ�Ȼ��̵Ĺ�������(���ֲ�����������)��
I������̷��м������ᣬ������Һ��pHԼΪ5���ⶨ���ӵij�ʼŨ�ȡ�����һ��ʱ����̷�������ʣ�࣬���ˣ�
II����I����Һ�м���һ�������ᣬ�ټ���![]() ��Һ����ַ�Ӧ�����
��Һ����ַ�Ӧ�����![]() ���������Һ��pHԼΪ5�����ˣ�
���������Һ��pHԼΪ5�����ˣ�
III����II����Һ��ͨ��![]() ���壬����ַ�Ӧ�����һ��ʱ�䣬��ȴ����ˣ�
���壬����ַ�Ӧ�����һ��ʱ�䣬��ȴ����ˣ�
IV��Ũ�����ᾧ�����ˡ�ϴ�ӡ���ˮ�õ���ˮMnCl2��
�������ж��������ӵ�ȥ�����
|
|
| |
��ʼŨ��/mg��L�C1 | 21.02 | 4.95 | 5.86 |
����I��/ mg��L�C1 | 12.85 | 3.80 | 3.39 |
����II��/ mg��L�C1 | 0.25 | 3.76 | 3.38 |
����III��/ mg��L�C1 | 0.10(���) | 3.19(��) | 0.12(���) |
��֪���������Mn��Fe��Ni��Pb
(1)�̺����ᷴӦ�Ļ�ѧ����ʽ��_______��
(2)����I��
��Fe2+Ũ�Ƚ��������д���![]() ��������ӷ���ʽ����ԭ��_______��
��������ӷ���ʽ����ԭ��_______��
��Pb2+Ũ�Ƚ��ͣ���������I�з����ķ�ӦΪ��Pb + 2H+ = Pb2+ + H2����______��
(3)����II��
��![]() ������Һ�����ã�_______��
������Һ�����ã�_______��
�ڽ�����ӷ���ʽ˵��MnCO3�����ã� _______��
(4)����IIIͨ��H2S�� Ni2+������![]() ��ꡣ�Ʋ��ܽ�ȣ�PbS_____NiS���>����<������
��ꡣ�Ʋ��ܽ�ȣ�PbS_____NiS���>����<������
(5)�ⶨ��ˮ![]() �ĺ�������a g ��Ʒ����һ�������������Ļ����Һ�У������Թ���
�ĺ�������a g ��Ʒ����һ�������������Ļ����Һ�У������Թ���![]() ��ʹ
��ʹ![]() ����Ϊ
����Ϊ![]() ������ַ�Ӧ���������һ��ʱ�䣬��ȴ����b mol/L���������
������ַ�Ӧ���������һ��ʱ�䣬��ȴ����b mol/L���������![]() �ζ�
�ζ�![]() ������c mL ��������李�����֪���ζ������з����ķ�ӦΪ��Fe2+ + Mn3+ = Fe3+ + Mn2+��
������c mL ��������李�����֪���ζ������з����ķ�ӦΪ��Fe2+ + Mn3+ = Fe3+ + Mn2+��
����Ʒ��MnCl2������������_____����֪��MnCl2��Ħ��������126 g��mol-1����
�ڡ��������ȡ���Ŀ����ʹ������![]() �ֽ⡣�������ȣ��ⶨ�����______���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�ֽ⡣�������ȣ��ⶨ�����______���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
����Ŀ��NaNO2�dz��õ�һ�ַ�����������+3�۵�N����һ���������ԡ�ijʵ��С���������·�Ӧ2NO2+2NaOH=NaNO3+NaNO2+H2O�Ʊ�NaNO2����̽�������ʡ�
I.�Ʊ�NaNO2
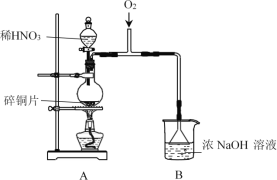
(1)A�з�����Ӧ�Ļ�ѧ����ʽ��______��
(2)B��ѡ��©�������ֱ���ܵ��ŵ���______��
(3)Ϊ����B���Ƶ�NaNO2����������ʵ�飺
��� | �Թ� | ���� | ���� |
�� | 2mLB����Һ | ��2mL0.1mol/LKI��Һ���μӼ��ε�����Һ | ������ |
�� | 2mLB����Һ | �μӼ���H2SO4��pH=5����2mL0.1mol/LKI��Һ���μӼ��ε�����Һ | ���� |
�� | 2mLH2O | �μӼ���H2SO4��pH=5����2mL0.1mol/LKI��Һ���μӼ��ε�����Һ | ������ |
ʵ��۵�Ŀ����_______��
(4)����Ϊ����3��ʵ����֤��B��һ����NaNO2�����貹��ʵ�飬������______��
II.̽��NaNO2������
װ�� | ���� | ���� |
| ȡ10mL1mol/LNaNO2��Һ���Լ�ƿ�У����뼸��H2SO4�ữ���ټ���10mL1mol��L-1FeSO4��Һ��Ѹ����������������ͨ������O2�� | i.��ҺѸ�ٱ�Ϊ��ɫ�� ii.��Һ��dz������ɫ���ݲ�������Һ�Ϸ�Ϊdz����ɫ�� iii.�����γ��غ�ɫ��Һ�� |
���ϣ�i.
ii.HNO2����Һ�в��ȶ����ֽ����NO��NO2���塣
(5)����i��Һ��Ϊ��ɫ��ԭ����______��
(6)��֪����ii��ɫ��Һ��dz������������Fe3+����Ӧ�����ӷ���ʽ��______��